Descrizione delle tipologie di prodotti contenenti ingredienti botanici presenti sul mercato nazionale e internazionale
Introduzione
I prodotti contenenti ingredienti botanici (spesso citati con la terminologia inglese botanicals) trovano un largo consenso nella popolazione generale e sempre più entrano a far parte delle abitudini dietetiche quotidiane. I prodotti con ingredienti vegetali o loro derivati rientrano in varie categorie, che possono essere regolamentate diversamente nei vari Paesi, inclusi quelli appartenenti all’Unione Europea. Una possibile classificazione dei prodotti contenenti ingredienti botanici e la relativa legislazione di riferimento vengono descritte in Figura 1.
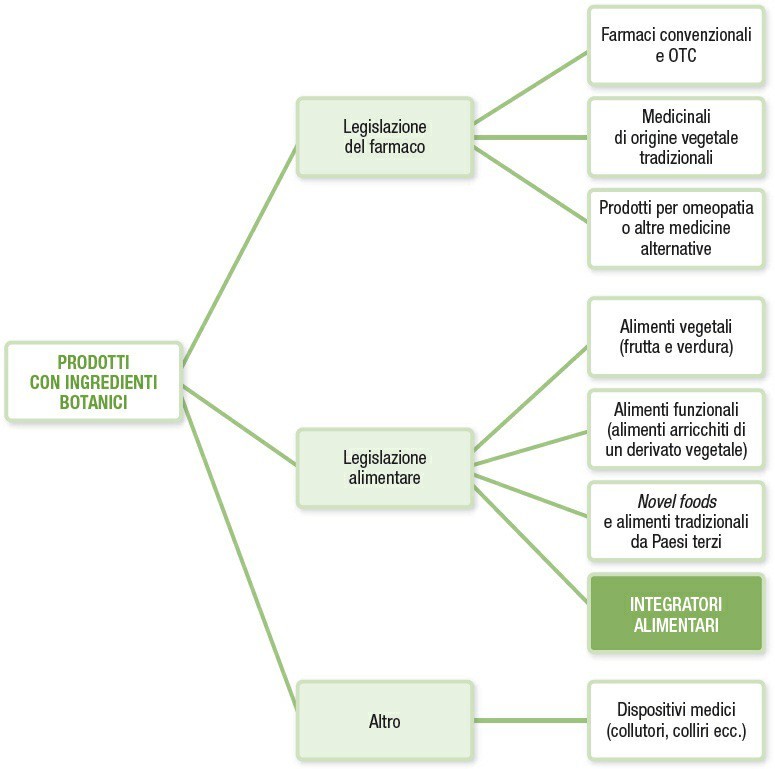
Figura 1. Una possibile classificazione dei prodotti contenenti ingredienti botanici e la relativa legislazione di riferimento.
Prodotti regolamentati dalla legislazione del farmaco
Principi attivi di origine vegetale sono da lungo tempo conosciuti e utilizzati nella medicina convenzionale (principi attivi estratti da digitale, valeriana, tasso ecc.), ma sempre più è andato diffondendosi l’uso di piante e derivati nella medicina alternativa, che non sempre viene riconosciuta dalla comunità scientifica. Va sottolineato, come descritto di seguito, che alcuni Paesi europei (ad esempio la Germania) propendono per l’inclusione dei botanicals nella categoria dei medicinali vegetali tradizionali che possono essere utilizzati senza prescrizione e supervisione del medico. La registrazione dei farmaci tradizionali risulta semplificata e si basa
fondamentalmente sulla tradizione d’uso, per cui si consente di limitare la sperimentazione clinica qualora ci siano dati che assicurino la sicurezza per il consumatore nelle condizioni d’uso previste. I prodotti inquadrati nella normativa del farmaco non verranno considerati in questo capitolo, in quanto non rientrano negli obiettivi della trattazione.
Dispositivi medici
Gli ingredienti botanici possono essere contenuti anche in prodotti rientranti nella categoria dei dispositivi medici; ne sono alcuni esempi:
- alcune soluzioni oftalmiche idratanti che contengono per lo più camomilla, calendula, fiordaliso ma anche eufrasia e mirtillo;
- alcuni liquidi utilizzati nella cura delle lenti a contatto, che includono tra gli altri arabinogalattani ed estratti di cellule staminali vegetali;
- alcuni collutori utilizzati per il trattamento delle infiammazioni gengivali e delle afte. Tra i vari possibili ingredienti di origine vegetale impiegati a questo scopo possono essere ricordati camomilla, aloe e
Anche i dispositivi medici non verranno descritti in dettaglio, essendo esclusi dalle categorie di interesse di questa trattazione.
Prodotti regolamentati dalla legislazione alimentare
Le categorie di prodotti appartenenti a questo gruppo sono in crescita e ne verrà fatta per ciascuna una breve descrizione.
Alimenti di origine vegetale
Si tratta principalmente di frutta e verdura commercializzate come tali o in forma di preparazione (confetture, marmellate, purea ecc.). Fanno parte della nostra comune dieta e nella maggior parte dei casi sono utilizzati da moltissimi anni/secoli. Meno frequentemente, l’uso può essere recente e in genere dipende dall’importazione di “nuovi” frutti o verdure tipici di zone geografiche lontane dall’area Mediterranea (kiwi dalla Nuova Zelanda, frutta esotica proveniente dai Paesi tropicali ecc.).
Alimenti arricchiti o funzionali
Pur non esistendo una definizione universalmente riconosciuta, quando si parla di un alimento funzionale si intende un prodotto a cui sia stato addizionato (o più raramente sottratto) uno o più ingredienti, con un’azione positiva (o negativa come nel caso di un allergene) sulla funzionalità di un organo o sistema. Si tratta quindi di un alimento che non ha solo la funzione di apportare calorie e nutrienti, ma che intende svolgere un’azione favorevole sulla salute del consumatore. Tale effetto deve essere compatibile con la quantità di alimento comunemente consumata, deve essere in forma “tradizionale” (e non in forma predosata) e deve garantire la sicurezza dei soggetti che assumono il prodotto, anche qualora presentino comuni patologie. Diffusi sono gli ingredienti prebiotici, ovvero quelle fibre solubili in grado di promuovere la crescita del microbiota intestinale positivo; le fibre più utilizzate sono l’inulina e i frutto-oligosaccaridi (da
cicoria o topinambur).
Novel foods e alimenti tradizionali da Paesi terzi
A livello europeo la regolamentazione dei nuovi alimenti, ovvero dei novel foods, è stata modificata nel 2015 (Regolamento UE 2015/2283). Rispetto alle normative precedenti, la definizione degli stessi è stata comunque mantenuta: “prodotti o sostanze alimentari privi di storia di consumo al 15 maggio 1997 in Europa”. Prima della loro commercializzazione, va fornita opportuna documentazione al fine di dimostrarne la sicurezza. Questa categoria include anche i prodotti ottenuti con nuove tecnologie.
Il regolamento sopra citato ha introdotto una nuova procedura di autorizzazione per gli “alimenti tradizionali derivanti da Paesi terzi”, con la quale dicitura si intende un alimento di comprovata tradizione di uso sicuro in un Paese terzo per almeno 25 anni. Rispetto alla procedura dei novel foods, questa nuova categoria deve presentare una minore documentazione per l’approvazione.
Integratori alimentari
Per gli integratori alimentari esistono diverse definizioni stilate da vari organismi nazionali e internazionali. Riportiamo di seguito quella pubblicata sul sito del Ministero della Salute: gli integratori alimentari sono: “prodotti alimentari destinati ad integrare la comune dieta e che costituiscono una fonte concentrata di sostanze nutritive, quali le vitamine e i minerali, o di altre sostanze aventi un effetto nutritivo o fisiologico, in particolare, ma non in via esclusiva, aminoacidi, acidi grassi essenziali, fibre ed estratti di origine vegetale, sia monocomposti che pluricomposti, in forme predosate”.1 Stiamo parlando di prodotti in forma predosata (capsule, compresse, gocce ecc.) destinati a integrare la dieta, senza lasciar intendere che possano sostituirsi a un approccio alimentare e stili di vita corretti. Quest’ultima categoria sarà trattata in questo capitolo con maggior diffusione: saranno esclusi i prodotti che contengano esclusivamente vitamine e minerali (trattati altrove), mentre ci si focalizzerà su quelli che annoverano tra gli ingredienti piante o estratti delle stesse.
Integratori alimentari contenenti piante o estratti di piante Introduzione
Come già ricordato in precedenza, gli integratori alimentari contenenti piante o derivati hanno
trovato notevole diffusione e accettazione da parte del consumatore, che considera il termine “naturale” sinonimo di sicurezza. Questa convinzione spiega il successo di questi prodotti e quindi la loro consistente presenza sul mercato. Torneremo in seguito sul concetto di sicurezza per il consumatore, che deve ovviamente essere sempre garantita dal produttore, e sull’associato concetto di controllo di qualità degli integratori lungo tutta la filiera, esattamente come per tutti gli altri alimenti.
Piante ammesse dalle legislazioni nazionali e internazionali
Accanto alle differenze legislative già segnalate, esistono diverse problematiche relative agli integratori contenenti botanicals; certamente una delle più critiche è rappresentata dalle diverse liste di ingredienti ammessi. Sebbene da tempo si lavori per un’armonizzazione almeno a livello europeo, questo obiettivo non è stato ancora raggiunto. Molti Paesi dell’Unione Europea, ma anche di altri continenti, hanno stilato liste positive e/o negative di piante (e sostanze correlate) che sono ammesse o vietate negli integratori alimentari. In alcuni casi vengono anche definiti limiti per quelle molecole in grado di comportare problematiche per la salute del consumatore, come nel caso delle ammine attive del Citrus aurantium, di cui si parlerà di seguito. Ulteriori informazioni sulle liste di piante ammesse o meno nei vari Paesi europei e in quelli di altri continenti sono disponibili altrove.2
Va riconosciuto l’importante sforzo compiuto da tre Paesi europei nel tentativo di uniformare le proprie liste. In questo contesto Belgio, Francia e Italia hanno coniato l’acronimo BELFRIT a definire la lista condivisa di botanicals ammessi nella categoria degli integratori alimentari. Il progetto, che si è avvalso della collaborazione di esperti scientifici (uno per ogni Paese), aveva come obiettivo la compilazione e successiva adozione di una lista comune di ingredienti botanici derivante dal confronto di quelle presenti nei tre Paesi. L’armonizzazione delle liste nazionali è fondamentale per ottimizzare la tutela della salute dei consumatori e per favorire il libero scambio dei prodotti, almeno tra i Paesi membri della Comunità Europea.
Con il DM del 10 agosto 2018 e il Decreto Dirigenziale del 9 gennaio 2019, la lista delle piante ammesse in Italia negli integratori alimentari è stata aggiornata; nell’allegato 1 sono confluite le piante della lista BELFRIT non comprese nell’allegato 1 del DM 9 luglio 2012. La nuova lista elenca il nome botanico delle piante autorizzate, la famiglia di appartenenza, i sinonimi, le parti impiegate secondo la tradizione d’uso e le linee guida ministeriali per gli effetti fisiologici. In alcuni casi vengono riportate ulteriori indicazioni quali le raccomandazioni da riportare in etichetta (quali la richiesta del parere medico in caso di uso prolungato) e altre eventuali prescrizioni (quali i limiti massimi di alcune molecole con la dose giornaliera, come nel caso di Citrus aurantium).
Prospettive future
Da quanto detto in precedenza, è evidente che permangono alcune problematiche importanti, tra cui l’inclusione degli stessi ingredienti botanici in tipologie diverse di prodotti commerciali e la presenza non coerente dei vari ingredienti botanici nelle liste di piante ammesse o non ammesse. Questa situazione porta a difficoltà oggettive nella libera circolazione delle merci anche nell’area dell’Unione Europea; un esempio chiarificatore può derivare dalla situazione dell’ingrediente “ginseng” (Panax ginseng). Infatti, anche tenendo conto dei soli Paesi membri dell’Unione Europea, si osservano numerose incongruenze nell’inclusione del ginseng nelle diverse tipologie commerciali:2
- 21 Paesi lo ammettono negli integratori alimentari: 12 senza norme specifiche, 6 con limiti quantitativi, 3 con limiti nella formulazione (ad esempio il tipo di estratto);
- 4 Paesi usano la valutazione caso per caso del prodotto, tenendo conto dell’attività fisiologica prevista;
- 1 Paese prevede una formale autorizzazione pre-marketing;
- 1 Paese non lo ammette negli integratori ma nel farmaco
È chiaro, quindi, quanto sia difficile da parte dei produttori gestire un mercato in cui uno stesso ingrediente, o anche lo stesso prodotto, può essere venduto con classificazione (farmaco o integratore alimentare) e/o requisiti diversi nei Paesi dell’Unione Europea.
Le prospettive future non sono al momento ottimistiche; l’unica strada percorribile è quella di un’armonizzazione a livello internazionale o almeno europeo; purtroppo questo obiettivo sembra difficilmente perseguibile nel breve termine.
Utilizzo in Italia di integratori alimentari contenenti piante o estratti di piante
Introduzione
Definire con esattezza la consistenza del mercato italiano non è cosa facile e dipende dal tipo di dati di cui ci si avvale. Le fonti consultabili sono molte, tra le altre:
- il mercato delle materie prime, che ha però un grande limite nella difficoltà di differenziare i vari utilizzi (alimenti tal quali, piante vendute in erboristeria sfuse, integratori alimentari, farmaci convenzionali e tradizionali);
- il mercato degli integratori alimentari stessi, in cui si evidenziano alcune criticità: il numero elevato di punti vendita e l’oggettiva difficoltà nel verificare i prodotti non venduti, che possono restare sugli scaffali per alcuni anni;
- i dati derivanti direttamente dai consumatori, che però non possono essere considerati del tutto veritieri non potendo intervistare tutta la popolazione. I consumatori sono comunque un’importante fonte di informazioni sul reale consumo, in quanto si può escludere la quota di prodotti acquistata ma non
Le informazioni sull’utilizzo degli integratori con ingredienti botanici in Italia, riportate in questo capitolo, si basano sulle seguenti fonti: i dati forniti dall’agenzia New Line e i risultati dell’indagine effettuata in 6 Paesi europei, inclusa l’Italia, nell’ambito del progetto Europeo PlantLIBRA.3 Per questa ultima fonte, si approfondiranno i dati raccolti nelle 4 città arruolate nel territorio italiano.4
I dati di New Line ricerche di mercato
In uno scenario italiano nel quale la domanda di salute e prevenzione, unitamente all’aspettativa di vita, cresce costantemente (dati ISTAT), è sempre più rilevante l’approccio a un sano stile di vita e a una corretta integrazione per mantenere uno stato di benessere. A conferma di questa tendenza, il fatturato del comparto integratori alimentari (nel loro complesso) in farmacia ha registrato negli ultimi 6 anni un tasso di crescita media annua (CAGR) pari al 6,8%.
La farmacia è canale di elezione per la vendita di questa categoria di prodotti, trattati anche da parafarmacia e grande distribuzione (GDO); nel corso degli ultimi 12 mesi si è raggiunto un fatturato di 2,8 miliardi di euro con un profilo di crescita del 3,9% (aggiornamento dati ad aprile 2019). Questo canale da solo genera l’84% del fatturato sviluppato dai tre canali, pari a 3,4 miliardi di euro (+3,9% negli ultimi 12 mesi).
Sempre nel contesto farmacia, i botanicals, ovvero integratori con componente attiva di origine vegetale, convogliano oltre il 16% del fatturato, realizzando più di 469 milioni di euro. Tuttavia, l’andamento delle vendite è del –2,2%, in controtendenza rispetto all’intero settore.
Dati raccolti dal Progetto Europeo PlantLIBRA
L’indagine condotta dal Progetto PlantLIBRA3 ha consentito di ottenere numerosissime informazioni relativamente ai consumatori di integratori a base di piante. Lo studio ha coinvolto 2400 persone reclutate in 6 Paesi europei (400 per Paese), a partire da circa 12.000 soggetti adulti contattati. L’indagine ha coinvolto 4 città per ogni Paese, scelte in base alla localizzazione geografica; in Italia le città coinvolte sono Milano, Venezia, Roma e Catania. I dati italiani verranno parzialmente riportati in questo capitolo; per ulteriori dettagli è possibile riferirsi al lavoro di Restani et al.4
La numerosità, l’età e le caratteristiche socio-economiche dei consumatori inclusi nell’indagine italiana sono riportate nella Tabella 1. Va sottolineato che i valori percentuali riferiti alla prevalenza di consumatori in Italia hanno dei limiti concreti, essendo stati calcolati su una quota relativamente bassa di abitanti. Lo studio ha consentito però di ottenere molte informazioni sui consumatori di integratori a base di erbe, con la specificità delle diverse zone geografiche: nord (Milano), nord-est (Venezia), centro (Roma) e sud-Isole (Catania). Il numero di arruolati e la loro distribuzione per sesso e fasce di età sono sovrapponibili nelle 4 città, come atteso dai criteri previsti per l’arruolamento: 400 arruolati (circa 100 per città), circa 50% maschi/femmine, 70% tra 18 e 59 anni. Per quel che riguarda il livello di istruzione, in Italia e nelle 4 città la maggioranza degli arruolati ha un titolo di studio di scuola secondaria; Catania ha incluso un maggior numero di laureati rispetto alle altre città (37% contro circa 17%). Per quanto riguarda l’occupazione, la maggior parte dei consumatori è costituita da impiegati (51-64%) e pensionati (11-16%). A parte la minor presenza di studenti nella città di Milano (5% contro 12-17%), non sono state osservate importanti differenze.
abella 1.

Caratteristiche del campione di consumatori italiani incluso nello studio del Progetto Europeo PlantLIBRA
I consumatori potevano segnalare fino a 5 prodotti utilizzati; i dati riportati nelle Tabelle 2 e 3 si riferiscono quindi alle percentuali di tutti gli integratori segnalati.
Le ragioni d’uso, i principali luoghi d’acquisto e le fonti di informazioni sono illustrati in Tabella 2. Le tre ragioni d’uso più citate in Italia in ordine decrescente sono funzioni digestive (19%), attività tonica-energetica (15%) e proprietà rilassanti (11,5%). Nelle 4 città questa graduatoria viene conservata, con alcune eccezioni: Milano ha indicato al terzo posto l’azione sul sistema immunitario, Venezia al secondo posto segnala i prodotti per il controllo del peso corporeo.
abella 2.

Principali ragioni d’uso, luoghi di acquisto e fonti di informazioni per città espressi come percentuali di tutti gli integratori segnalati§
I principali luoghi d’acquisto di integratori alimentari con ingredienti botanici in Italia sono le erboristerie e i negozi similari (65% contro il 54% della situazione riscontrata nei 6 Paesi europei). Più in dettaglio, i punti vendita più frequentemente segnalati dai consumatori italiani sono erboristeria/parafarmacia (65%), farmacia (23,7%) e supermercato (7,9%). Anche in questo caso, le segnalazioni nelle 4 città sono sovrapponibili, a parte Milano che colloca al terzo posto, a pari merito, internet e la fornitura da parte di amici/parenti.
I consumatori italiani chiedono informazioni preferibilmente al responsabile della erboristeria/parafarmacia (34,8%) e ad amici/parenti (30,7%) Il 14,9% dichiara di compiere scelte autonome senza consigli specifici. La situazione nelle 4 città è simile con qualche variante:
al terzo posto Roma pone il farmacista e Catania il medico di famiglia. Le ragioni del maggior ruolo dell’erborista in Italia dipendono probabilmente dalla presenza di lauree nel settore (Scienze erboristiche), fatto che determina la competenza e, quindi, la confidenza del consumatore nei responsabili di questi punti vendita.
Le dieci piante più presenti negli integratori segnalati dai consumatori Italiani sono elencate in Tabella 3: tra queste, è interessante notare che solo una (il carciofo) compare nella lista delle “top 10” dell’intera indagine. Ai primi tre posti in Italia si collocano aloe, finocchio e valeriana, ma valutando le 4 città incluse nello studio si osservano variazioni significative. Ad esempio, i consumatori di Venezia hanno segnalato al primo posto il tarassaco; a Milano, Roma e Catania la terza posizione della valeriana viene occupata da un’altra pianta, diversa da città a città.
abella 3.

Le 10 piante più utilizzate per città espresse come percentuale di tutti gli integratori segnalati§
Cercando di trarre conclusioni dai dati riportati, si può dire che l’Italia presenta alcune peculiarità rispetto alle altre nazioni incluse nello studio, sia per quel che riguarda le piante più comunemente acquistate sia per i punti vendita e le figure di riferimento.
A che punto siamo con l’ottenimento dei claim salutistici? La situazione europea
La situazione poco coerente del mercato europeo degli integratori con ingredienti botanici porta inevitabilmente a conseguenze di vario tipo, tra cui la difficoltà nel discriminare informazioni “salutistiche” o “terapeutiche” per la stessa pianta usata in classi di prodotti diversi. Sappiamo che quel che fa la differenza è la dose, ma discriminare la dose con effetti fisiologici da quella idonea a curare è un’impresa complicata anche per le piante di più antica tradizione.
Se il prodotto è un farmaco, ci sono precise regole da seguire prima della commercializzazione relativamente a efficacia, qualità e sicurezza. Per i prodotti inquadrati nella “medicina tradizionale” esiste una via semplificata alla commercializzazione, che accetta a supporto del dossier di autorizzazione la tradizione d’uso, o meglio la “lunga” tradizione d’uso sia in Europa sia in Paesi terzi. In questo settore è indispensabile garantire la qualità e la sicurezza, ma non sono richiesti studi particolarmente complessi per dimostrarne l’efficacia.5
Nel caso degli integratori alimentari vale la regolamentazione dei prodotti alimentari, ma sono utilizzabili solo quegli ingredienti inclusi nelle liste di piante ammesse, come descritto al punto
2. Laddove si voglia utilizzare un claim (indicazione) nutrizionale quale guida per il consumatore, si deve far riferimento al Regolamento Europeo n. 1924/2006,6 secondo cui: “La fondatezza scientifica dovrebbe essere l’aspetto principale di cui tenere conto nell’utilizzo di indicazioni nutrizionali e sulla salute, e gli operatori del settore alimentare che fanno uso di indicazioni dovrebbero giustificarle”. Per ottenere l’autorizzazione ad associare un claim salutistico a un integratore alimentare, l’azienda produttrice deve presentare un dossier all’EFSA (European Food Safety Authority) che valuta l’evidenza scientifica degli studi forniti e pubblica un’opinione. Le linee guida fornite da EFSA descrivono in dettaglio gli studi richiesti per l’approvazione dei claim nutrizionali/fisiologici.7
Esistono due tipologie di frasi salutistiche, quelle relative all’art. 13 e quelle relative all’art. 14 del Regolamento europeo sopra citato (Regolamento 1924/2006). Le indicazioni “funzionali generiche” di cui all’articolo 13, paragrafo 1 riguardano il ruolo positivo che una sostanza nutritiva, o di altro tipo, può avere sulla crescita, lo sviluppo e le funzioni dell’organismo, sulle funzioni psicologiche e comportamentali, sul dimagrimento e il controllo del peso, sul senso di sazietà o sulla riduzione dell’energia apportata dal regime alimentare. Queste indicazioni non comprendono quelle riferite alla riduzione del rischio di malattia e allo sviluppo o salute dei bambini, che vengono invece regolate dall’art. 14.
Le linee guida pubblicate da EFSA, pur estremamente ben articolate, hanno portato però a immediate difficoltà nella realizzazione di un dossier che potesse rispondere a tutti i requisiti elencati. Tra gli aspetti più critici e importanti:
- parlando di integratori alimentari non si può vantare alcun effetto terapeutico ma solo fisiologico; ne consegue che, a parte poche eccezioni, è molto difficile dimostrare una funzione salutistica che ha l’obiettivo di mantenere l’omeostasi o ridurre i fattori di rischio di malattia nel lungo termine;
- per ottenere significatività statistica è necessario arruolare una popolazione “sana” molto numerosa che sia disponibile ad assumere un certo prodotto per periodi molto lunghi. Tutto questo risulta economicamente poco sostenibile e i risultati potrebbero comunque essere inficiati dalle abitudini alimentari (e non solo) dei soggetti considerati;
- sembra poco ragionevole che la tradizione d’uso sia accettata per i farmaci di medicina tradizionale e non per gli integratori
A conferma delle oggettive difficoltà nell’ottenere un’autorizzazione alle frasi salutistiche basti pensare che delle 2337 richieste pervenute a EFSA (a maggio 2019), solo 261 sono state
autorizzate e di queste solo 13 si riferiscono chiaramente a una pianta: dieci riguardano l’articolo 13 e tre l’articolo 14. La Tabella 4 elenca solo 7 voci perché sono state aggregate quelle analoghe (ad esempio le fibre). A quanto riportato in Tabella 4 vanno poi aggiunte alcune frasi ammesse per ingredienti di origine vegetale come gli steroli e stanoli, di cui però non si specifica la precisa origine botanica. Va infine fatto osservare che il parere positivo riguarda in due casi la frutta (prugne secche e noci) e in un altro l’olio di oliva.
abella 4. Informazioni nutrizionali/salutistiche autorizzate da EFSA per ingredienti botanici

Definite le principali criticità e la situazione attuale delle frasi ammesse, va sottolineato che gli integratori alimentari contenenti piante sono comunque in commercio e in libera vendita; questo significa che, in assenza di indicazioni al consumatore, si potrebbero verificare usi incongrui, se non pericolosi.
La situazione italiana
Con il DM del 10 agosto 2018 e il Decreto Dirigenziale del 9 gennaio 2019, l’Italia ha aggiornato la lista delle piante ammesse negli integratori alimentari, ma è andata oltre. Tenendo conto della necessità di garantire la salute del consumatore, il Ministero della Salute ha scelto di indicare, nella lista delle piante ammesse, quelle frasi che hanno lo scopo di guidare nella scelta dei prodotti e che si riferiscono esclusivamente all’ottimizzazione delle funzioni dell’organismo nell’ambito dell’omeostasi. Queste frasi derivano da dati provenienti dalla tradizione d’uso e saranno permesse fino a ulteriori decisioni a livello europeo.
Qualità e sicurezza degli integratori alimentari contenenti
botanicals
Il ruolo della qualità nella sicurezza
La qualità di un prodotto alimentare è sempre un requisito fondamentale per la sicurezza del consumatore. Gli integratori contenenti piante sono alimenti e quindi devono osservare la legislazione del settore in termini di produzione e controllo; la presenza di ingredienti botanici aggiunge però qualche criticità specifica. Un breve articolo su questo argomento è stato preparato nell’ambito del Progetto PlantLIBRA e fornisce alcune informazioni che verranno qui solo parzialmente riprese.8 La Figura 2 riassume gli aspetti che in diverso modo concorrono alla qualità dei prodotti e alla sicurezza del consumatore. Gli attori sono molti e non si limitano all’azienda produttrice; oltre all’agricoltore, che è responsabile della materia prima, il consumatore stesso può essere responsabile di comportamenti che possono compromettere il corretto uso degli integratori alimentari.

Figura 2. Fattori che intervengono nella qualità dei prodotti contenenti piante e relativa ricaduta sulla sicurezza del consumatore.
La materia prima rappresenta il primo stadio della filiera e ha un ruolo cruciale nella qualità; le piante che verranno utilizzate come ingredienti, indipendentemente dalla strategia agronomica scelta (agricoltura convenzionale, biologica, lotta integrata), dovranno essere sottoposte a stretti controlli per i contaminanti biologici (batteri, virus, muffe e relative tossine) e chimici (pesticidi, metalli pesanti ecc.). Per ridurre al massimo i rischi per il consumatore, gli agricoltori devono seguire le norme di Buone Pratiche Agricole (GAP) per l’uso di pesticidi o fertilizzanti o adeguarsi alla normativa per l’agricoltura biologica. Il produttore sarà responsabile delle Buone Pratiche di Produzione che prevedono un controllo ulteriore della materia prima e la garanzia della qualità finale che, nel caso degli ingredienti botanici, prevede anche un titolo in componenti attivi, ovvero le sostanze ritenute responsabili dell’effetto fisiologico voluto. Per fare qualche esempio, l’Artiglio del diavolo (Harpagophytum procumbens) deve riportare il titolo di arpagoside, l’Aloe (Aloe vera) in aloina A e B, il Ginkgo (Ginkgo biloba) in ginkgoflavonglucosidi ecc.
In etichetta devono essere indicati anche i contenuti di alcune classi di molecole che sono regolamentate da direttive nazionali o internazionali o circolari ministeriali, come ad esempio nel caso dell’arancio amaro (Citrus aurantium) per cui è necessario dichiarare il contenuto di sinefrina e delle altre ammine attive apportate con la dose giornaliera. Si tratta di solito di molecole che a livelli elevati possono comportare effetti collaterali non desiderati e quindi vanno “normate” le dosi giornaliere sicure per il consumatore.
Va sottolineato che qualunque controllo di qualità può perdere significato se il consumatore assume gli integratori senza opportuna consapevolezza. Si è detto che gli integratori alimentari vanno a integrare la dieta e non possono sostituire una sana alimentazione. I prodotti contenenti piante hanno inoltre ingredienti con una funzione fisiologica su particolari organi/sistemi e il consumatore deve acquistare sulla base dell’effetto ricercato. In questo senso, come detto in precedenza, risulta controverso l’atteggiamento di divieto di qualunque informazione “salutistica” se non a seguito di un’opinione positiva dell’EFSA. Sebbene sia fondamentale che quanto si scrive in etichetta sia realistico sulla base di dati scientifici, è anche vero che senza alcuna indicazione il consumatore si trova nell’incertezza della scelta e a rischio di uso inadeguato.
Gli eventi avversi
Molto importante risulta l’informazione fornita sia alla popolazione generale sia ai soggetti a rischio: tutti devono sapere che a seguito del consumo di ingredienti botanici si possono manifestare eventi avversi. È importante ricordare che le donne in gravidanza o in allattamento dovrebbero attenersi strettamente alle indicazioni del medico e che nei bambini l’uso di prodotti con derivati delle piante deve essere escluso, a parte prodotti specificamente studiati e comunque consigliati dal pediatra. Particolare attenzione dovranno poi mostrare i consumatori con patologie associate all’alimentazione, quali per esempio i celiaci e gli allergici.
Le maggiori criticità, relative agli eventi avversi, risiedono nel fatto che il consumatore medio ritiene il “naturale” sicuro e pertanto non considera i prodotti botanici come possibile fonte di malessere; inoltre, raramente ne comunica al medico l’utilizzo in caso di terapia a breve o lungo termine.
Dalla raccolta di dati effettuata durante e dopo il progetto europeo PlantLIBRA, è stato possibile identificare le principali tipologie di eventi avversi associati agli integratori con ingredienti botanici; le manifestazioni cliniche variano in relazione alla pianta considerata e al relativo utilizzo (dose, scopo fisiologico ecc.). I dati nel loro complesso sono stati pubblicati da Di Lorenzo et al.9 e, oltre a tutti i dati prodotti da PlantLIBRA, includono le segnalazioni ricevute dal Centro antiveleni di Pavia dopo la conclusione del progetto, dalla Nutrivigilanza di ANSES (Agenzia francese per la sicurezza degli alimenti) e dall’FDA (US Food and Drug Administration).
Nel lavoro citato9 sono stati quindi elaborati i dati ottenuti da 6 fonti diverse: letteratura scientifica, indagine PlantLIBRA su 30 centri antiveleno europei, centro antiveleno di Pavia (post-progetto), indagine PlantLIBRA sul consumatore, nutrivigilanza di ANSES e FDA. Valutando complessivamente i risultati ottenuti, si è osservato che il tè verde (Camellia sinensis) e il ginseng (Panax ginseng) appaiono tra le tredici piante più citate per eventi avversi, in tutte le liste a parte FDA. La valeriana (Valeriana officinalis) è inclusa in 4 su 6 liste; arancio amaro (Citrus aurantium), carciofo (Cynara scolimus), ginkgo (Ginkgo biloba), soia (Glicine max), liquirizia (Glycyrrhiza glabra), melissa (Melissa officinalis) e guaranà (Paulinnia cupana) appaiono in 3 su 6 liste. L’entità dell’evento avverso può essere estremamente variabile: da gravità bassa o moderata a, seppur rari, eventi fatali.
Molto importante risulta la consapevolezza del consumatore sulla possibile interazione tra gli integratori contenenti piante e i farmaci tradizionali; sono state descritte interazioni con sintomatologia severa tra integratori contenenti riso rosso e statine (aumento del rischio di rabdomiolisi, ovvero l’effetto collaterale delle statine), tra liquirizia e farmaci antipertensivi (effetto antipertensivo ridotto), tra valeriana e farmaci sedativi (potenziamento dell’effetto) ecc. Per un approfondimento sui possibili effetti collaterali e soprattutto delle interazioni con farmaci si rimanda ad altri lavori.4,9,10,11
Qualche esempio
Considerando l’elevatissimo numero di piante ammesse negli integratori alimentari non è possibile dare una visione di insieme del settore. Si descriveranno pertanto, a titolo di esempio, le caratteristiche di quattro piante che sono risultate frequentemente presenti negli integratori alimentari segnalati dai consumatori italiani dell’indagine di PlantLIBRA.3,4
Camellia sinensis (L.) Kuntze – tè verde
La Camellia sinensis, comunemente nota come tè, è una pianta della famiglia delle Theaceae. È inclusa dal Ministero della Salute nella lista delle piante ammesse negli integratori alimentari e la parte utilizzabile è rappresentata dalle foglie. Ne esistono tre principali tipologie: il tè verde, il tè nero e il tè oolong.
La particolarità del tè verde risiede nella sua modalità di manipolazione una volta effettuato il raccolto. Le foglie vengono lasciate avvizzire all’aria in modo da eliminare gran parte del contenuto d’acqua e poi vengono sottoposte a un processo di stabilizzazione per calore. Questo procedimento ha come obiettivo quello di impedire il processo di ossidazione e mantenere il colore, l’aroma e la composizione chimica. Nel caso del tè nero, la lavorazione delle foglie consiste in una prima fase di appassimento dove il naturale processo di fermentazione viene incrementato con la rollatura. A ciò segue la fase ossidativa, che dura circa 5 ore e comporta la modifica del colore, che imbrunisce, e del gusto, che assume un carattere pungente e penetrante. Il tè oolong è un prodotto intermedio tra il tè verde e il tè nero. Dopo l’iniziale fase di appassimento, all’aria aperta, si esegue un processo di ossidazione più breve rispetto al tè nero con conseguente modifica intermedia dei componenti attivi. La maggior parte degli integratori alimentari include estratti di tè verde, ovvero foglie che non hanno subìto ossidazione; questi estratti, rispetto a quelli da tè nero, sono più ricchi in molecole attive (catechine).
Tradizione d’uso e componenti attive
Il tè ha una lunga tradizione d’uso; le prime descrizioni risalgono alla Dinastia Song cinese (960- 1279), ma il suo consumo ha raggiunto la massima diffusione dapprima in Giappone e poi in tutto il mondo grazie al suo arrivo in Europa nel 1610 con la Compagnia Olandese delle Indie Orientali.12 Le linee guida ministeriali riportano quale riferimento fisiologico per la Camellia sinensis: “Drenaggio dei liquidi corporei, equilibrio del peso corporeo, normale funzionalità intestinale, tonico (stanchezza fisica, mentale), antiossidante”. Il tè contiene moltissime molecole attive, prima fra tutte la caffeina (teina), che attribuisce a questa bevanda l’attività positiva sull’attenzione e sulla stanchezza. Gli effetti antiossidanti, e in generale salutistici, sono associati al contenuto in polifenoli, di cui i più abbondanti appartengono alle classi dei flavanoli e flavonoli.13 Particolarmente attiva è l’epigallocatechina 3-gallato (EGCG), che costituisce la catechina più abbondante del tè verde e un composto minore del tè nero. Questo giustifica il fatto che gli integratori siano quasi esclusivamente a base di estratti di tè verde.
Health claim
L’EFSA14 ha valutato complessivamente le richieste dei seguenti claim salutistici per il tè riferiti all’Articolo 13:
- contributo al mantenimento o raggiungimento di un peso corporeo normale;
- aumento della beta-ossidazione degli acidi grassi con associata riduzione della massa grassa;
- mantenimento dei normali livelli di
In tutti i casi, il Panel NDA (Dietetic Products, Nutrition and Allergies) dell’EFSA ha concluso che, sulla base dei dati forniti, non era possibile stabilire una correlazione tra il consumo di catechine da tè verde e gli effetti dichiarati.
Problematiche associate al corretto consumo
L’uso del tè verde come infuso e come ingrediente di integratori alimentari è stato oggetto di un’altra opinione dell’EFSA15 che ha valutato la possibile correlazione tra il consumo di EGCG e gli effetti epatotossici riportati nel tempo in diversi Paesi. Dalla documentazione scientifica raccolta, l’EFSA si è espressa nel seguente modo:
- il contenuto di catechine presenti negli infusi preparati nel modo tradizionale (o in bevande ricostituite a partire da tali infusi disidratati) va considerato sufficientemente sicuro sulla base del consumo di questi prodotti nei Paesi europei; i rari casi di epatotossicità segnalati a seguito di consumo di infuso di tè verde sono probabilmente da attribuire a reazioni idiosincratiche;
- per quel che riguarda gli integratori a base di estratti, si può affermare che dosi ≥800 mg di epigallocatechina gallato al giorno sono state associate in modo statisticamente significativo all’aumento di transaminasi plasmatiche, parametri associati a sofferenza epatica. Dal momento che non sono disponibili dati certi per dosaggi <800 mg, gli esperti non hanno potuto fissare una dose Questo significa che al momento esiste incertezza sulla quantità massima giornaliera di epigallocatechina gallato, contenuta negli integratori alimentari a base di tè verde, che risulti priva di effetti avversi.
Citrus aurantium var. amara L. – arancio amaro
Il Citrus aurantium, comunemente noto come arancio amaro, è una pianta della famiglia delle Rutaceae. La pianta è probabilmente originaria dell’India nord-orientale, da cui si è diffusa inizialmente in Giappone, Myanmar e Cina e quindi nel resto del mondo, raggiungendo l’Europa circa 1000 anni fa. L’arancio amaro in passato era impiegato quasi esclusivamente negli alimenti e nelle bevande per le sue proprietà acidificanti e aromatizzanti; oggi trova un ampio impiego anche nel settore dei botanicals.
L’arancio amaro è incluso dal Ministero della Salute nella lista delle piante ammesse negli integratori alimentari. Le parti utilizzabili sono i fiori, il frutto, il pericarpo, le foglie e i relativi oli essenziali.
Tradizione d’uso e componenti attive
Le linee guida ministeriali riportano riferimenti fisiologici ben declinati:
- per i fiori e relativi oli essenziali: rilassamento e benessere mentale, funzione digestiva ed eliminazione dei gas intestinali;
- per il frutto: funzione digestiva ed eliminazione dei gas intestinali;
- per il frutto immaturo: equilibrio del peso corporeo, stimolo metabolico e metabolismo dei lipidi, funzione digestiva, regolare motilità gastrointestinale ed eliminazione dei gas;
- per il pericarpo e relativo olio essenziale: funzione digestiva, regolare motilità gastrointestinale ed eliminazione dei
L’attività fisiologica del Citrus aurantium è giustificata dalla presenza di numerose molecole attive appartenenti a classi chimiche diverse. Numerose molecole appartengono alla classe dei flavonoidi, e tra questi i più abbondanti sono i flavanoni (esperidina e naringenina). Un’altra classe importante è costituita dagli alcaloidi fenil-etil-amminici, di cui la molecola più rappresentativa è la sinefrina, seguita da octopamina, tiramina, N-metil tiramina e ordeina.16 La sinefrina ha struttura molto simile a quella dell’efedrina e per questo motivo gli estratti di Citrus aurantium hanno ricevuto particolare interesse dopo il bando dei derivati dell’Ephedra dagli integratori per sportivi.
Health claim
Non risultano opinioni pubblicate dall’EFSA relativamente a indicazioni salutistiche riguardanti estratti di Citrus aurantium.
Problematiche associate al corretto consumo
Alcune perplessità sono state sollevate in relazione all’uso degli estratti di Citrus aurantium a causa della già citata similitudine della sinefrina con la molecola dell’efedrina. L’efedrina è la molecola ritenuta responsabile di un certo numero di eventi cardiovascolari, talora fatali, osservati in atleti che consumavano integratori contenenti derivati dell’Ephedra.17 Gli estratti di
- aurantium, e in particolare la sinefrina, sono stati quindi ampliamente indagati per i possibili rischi a carico del sistema cardiovascolare. In realtà, si è osservato che la piccola differenza nella struttura chimica è in grado di modificare in modo significativo l’affinità della sinefrina per il recettore adrenergico, riducendo in modo determinante gli effetti avversi in questo distretto. Sulla base di queste considerazioni i derivati del Citrus aurantium sono ammessi negli integratori, ma con alcune restrizioni che possono variare da Paese a Paese. In Italia, il Ministero
della Salute riporta che:
- l’apporto massimo di sinefrina con la dose giornaliera non deve superare i 30 mg, che corrispondono approssimativamente a 800 mg di estratto titolato al 4%;
- l’apporto massimo di octopamina, come indice della presenza naturale di altre ammine, non deve superare 1/8 di quello della
Ginkgo biloba L. – ginkgo
Il Ginkgo biloba, comunemente noto come ginkgo, è una pianta della famiglia delle Ginkgoaceae. Ha origini antichissime e cresce spontaneamente in Cina, sebbene non si conoscano esattamente le sue origini. In Giappone e in Cina è stata spesso coltivata nelle aree dei templi, in quanto considerata pianta sacra (www.agraria.org/coltivazioniforestali/ginkgobiloba.htm). La pianta può raggiungere altezze ragguardevoli (anche 40 metri); ha chioma piramidale e foglie a tipica forma flabelliforme, ovvero di ventaglio. Come già indicato in precedenza per il Panax ginseng, i Paesi membri della UE non hanno posizione univoca sulla collocazione del ginkgo nelle diverse categorie di prodotti contenenti botanicals: 15 Paesi lo ammettono negli integratori alimentari ma 5 impongono limiti quantitativi e 3 restrizioni relative alla tipologia di preparato. In 7 Paesi il suo uso è vietato negli integratori, ma in alcuni casi può essere ammesso nei prodotti medicinali.2
Il ginkgo è incluso dal Ministero della Salute nella lista delle piante ammesse negli integratori alimentari; le parti utilizzabili sono le foglie e le gemme.
Tradizione d’uso e componenti attive
Il ginkgo ha una lunga tradizione d’uso nella medicina tradizionale; dati consolidati indicano che i preparati a base di foglie sono in grado di migliorare il decadimento cognitivo tipico dell’età avanzata e la qualità della vita nella demenza non grave. Nella medicina tradizionale è usato tipicamente per il sollievo della pesantezza alle gambe e della sensazione di freddo alle mani e ai piedi associabili a problemi circolatori minori.18 Le linee guida ministeriali riportano riferimenti fisiologici per le foglie: antiossidante, memoria e funzioni cognitive, normale circolazione del sangue, funzionalità del microcircolo.
L’attività degli estratti di Ginkgo biloba dipende principalmente dalla presenza di alcune molecole appartenenti alla classe dei lattoni terpenici: ginkgolide A, ginkgolide B e bilobalide. L’esatto meccanismo d’azione dei derivati di Ginkgo biloba sulle funzioni mnemoniche/cognitive non è del tutto chiaro, ma si ritiene che almeno in parte si basi sulla protezione delle cellule cerebrali dallo stress ossidativo, ovvero dall’azione tossica dei radicali dell’ossigeno.19
Health claim
Non risultano opinioni pubblicate dall’EFSA relativamente a indicazioni salutistiche riguardanti estratti di Ginkgo biloba.
Problematiche associate al corretto consumo
Alcune perplessità sono state sollevate in relazione all’uso degli estratti di Ginkgo biloba, in quanto sono stati segnalati casi di eventi avversi per lo più limitati a sanguinamento nasale o oculare; è però evidente che nei soggetti in terapia anticoagulante l’uso contemporaneo di estratti di ginkgo potrebbe determinare un evento emorragico più grave.10,19
Sulla base di queste considerazioni i derivati del Ginkgo biloba sono ammessi in Italia negli integratori, ma con alcune prescrizioni da riportare in etichetta:
- se si stanno assumendo farmaci anticoagulanti o antiaggreganti piastrinici, consultare il medico prima di assumere il prodotto;
- si sconsiglia l’uso del prodotto in gravidanza e durante l’allattamento.
Hypericum perforatum L. – iperico
L’Hypericum perforatum, comunemente noto come iperico o erba di San Giovanni, è una pianta della famiglia delle Hypericaceae, diffusa in tutta Europa. È stata considerata una pianta magica per molti secoli e il nome erba di San Giovanni deriva dal fatto che veniva usata in modo rituale nella notte del 24 giugno, dedicata a questo santo. È una pianta di altezza variabile (30-100 cm) con fiori di colore giallo dorato; le foglie presentano sulla superficie interna numerose ghiandole, per cui osservate contro luce appaiono finemente forate (www.agraria.org/coltivazioniforestali/erbe/erbemedicinali06.htm). Da quest’ultima caratteristica deriva il nome di “perforatum”.
L’iperico è incluso dal Ministero della Salute nella lista delle piante ammesse negli integratori alimentari; le parti utilizzabili sono la parte aerea con i fiori, i fiori e le sommità.
Tradizione d’uso e componenti attive
L’uso dell’iperico nella medicina tradizionale riguarda principalmente il miglioramento della stanchezza mentale temporanea, il trattamento di infiammazioni blande della pelle e delle ferite minori e il miglioramento di disturbi gastrointestinali.20,21 Le linee guida ministeriali riportano riferimenti fisiologici per le parti aeree con fiori: normale tono dell’umore, rilassamento e benessere mentale.
L’attività dell’iperico si basa su alcune molecole appartenenti a classi chimiche diverse: le più note sono l’ipericina (un antrachinone)22 e l’iperforina (un chetone terpenico ciclico).23 Altri composti dotati di attività fisio-farmacologica sono i flavonoidi, tra cui rutina, quercetina e kaempferolo. L’ipericina contribuirebbe all’effetto antidepressivo, inibendo la captazione neuronale di alcuni neurotrasmettitori, quali la serotonina, la noradrenalina, la dopamina, l’acido gamma ammino-butirrico e l’L-glutammato.22
Health claim
Non risultano opinioni pubblicate dall’EFSA relativamente a indicazioni salutistiche riguardanti, come tali, estratti di Hypericum perforatum. È stato invece considerato l’iperico in un’opinione riguardante diverse piante per le quali si richiedeva l’approvazione di una frase relativa al “supporto dei naturali meccanismi di purificazione dell’organismo e alla eliminazione di tossine”.14 Le conclusioni riferivano che la richiesta di opinione riguardava affermazioni troppo generiche per poter essere valutate dal Panel NDA.
Problematiche associate al corretto consumo
L’Hypericum perforatum va assunto con la consapevolezza dei possibili eventi avversi. Seppur non frequentemente, alcuni consumatori di iperico hanno manifestato effetti collaterali del tutto simili a quelli dei farmaci antidepressivi convenzionali: ansia, attacchi di panico, vomito, amnesia. Ancora più critica può essere l’assunzione di iperico in contemporanea con altri farmaci di cui può modificare la biodisponibilità; fra gli altri vanno citati gli antidepressivi, la pillola anticoncezionale e certi farmaci anticoagulanti. Va infine ricordato che l’assunzione di iperico in estate può portare a fotosensibilizzazione.
Sulla base di queste considerazioni i derivati dell’Hypericum perforatum sono ammessi in Italia negli integratori, ma con alcune prescrizioni:
- in etichetta va indicato l’apporto giornaliero di ipericina;
- in etichetta va riportata la seguente avvertenza supplementare: se si assumono farmaci, prima di utilizzare il prodotto chiedere il parere del medico perché l’estratto di iperico può interferire sul loro metabolismo, inibendone anche l’attività;
- l’estratto di iperico è controindicato in età pediatrica e nell’adolescenza.
Conclusioni
Il consumo di alcune piante, quali integratori della dieta, fa parte della tradizione d’uso di molti Paesi, inclusa l’Italia. Nonostante i numerosi dati rintracciabili nella letteratura scientifica, risulta però sempre complesso trovare una correlazione inequivocabile tra un effetto “fisiologico” e un certo prodotto contenente un ingrediente vegetale. Questa difficoltà nasce dal fatto che quantificare il “mantenimento dell’omeostasi” o la “riduzione dei fattori di rischio di malattia” in un soggetto sano è estremamente complesso, richiede tempi lunghissimi e un’alta numerosità della popolazione studiata, a cui corrispondono costi elevatissimi. Inoltre, risulta quasi impossibile in tempi lunghi eliminare i fattori confondenti, quali sedentarietà, peso corporeo, tabagismo, uso di farmaci ecc. Questo problema è sorto quando, nel tentativo di applicare il regolamento CE 1924/2006 sugli health claim, l’EFSA ha cominciato a valutare i dossier su prodotti contenenti botanicals.
Attualmente la situazione internazionale è confusa e non priva di contraddizioni:
- gli integratori alimentari sono presenti sul mercato europeo ma non potrebbero portare alcuna indicazione relativamente agli effetti ascrivibili agli ingredienti erboristici, se non dopo aver ottenuto un parere positivo dell’EFSA;
- al momento il numero di health claim ammessi per questa categoria di prodotti è trascurabile;
- i prodotti sono però egualmente sul mercato, in libera vendita. La potenziale mancanza di qualunque indicazione può essere fonte di erronee valutazioni da parte del consumatore poco informato, con conseguente rischio per la sua salute;
- su questo concetto l’Italia ha deciso di stilare linee guida (basate sulla tradizione d’uso) sugli effetti fisiologici che possono essere riportati in etichetta in attesa di ulteriori sviluppi a livello europeo.
Questa problematica deve essere affrontata e risolta rapidamente a livello internazionale, con spirito di collaborazione come quello mostrato in passato da Belgio, Francia e Italia nel progetto BELFRIT. È auspicabile che ci sia la volontà di armonizzare a livello internazionale le norme legislative e l’approccio scientifico alla valutazione delle indicazioni salutistiche, sempre tenendo presente l’importanza di informare e tutelare il consumatore.
Bibliografia
1. MINSAL 2019. www.salute.gov.it/portale/temi/p2_5.jsp? area=Alimenti%20particolari%20e%20integratori&menu=integratori
2. Coppens P, Pettman S. The regulatory situation in Europe and other continents. In: Food supplements containing botanicals: Benefits, side effects and regulatory aspects. The scientific inheritance of the EU Project PlantLIBRA, P. Restani Editor. Springer International Publishing AG, 2019:27-59.
3. Garcia-Alvarez A, Egan B, de Klein S, et al. Usage of plant food supplements across six European countries: findings from the PlantLIBRA consumer survey. PLOS One 2014;9: e92265.
4. Restani P, Di Lorenzo C, Garcia-Alvarez A, et al. Adverse effects of plant food supplements self- reported by consumers in the PlantLIBRA survey involving six European countries. PLoS One 2018;11: e0150089.
5. Larrañaga-Guetaria A. PlantLIBRA: plant food supplements, level of intake, benefit and risk assessment. The regulatory framework for plant food supplements in the EU. AgroFOOD Industry Hi- Tech 2012;23:20-2.
6. Comunità Europea 2006. Regolamento (CE) n. 1924/2006 del Parlamento europeo e del consiglio del
20 dicembre 2006 relativo alle indicazioni nutrizionali e sulla salute fornite sui prodotti alimentari. Gazzetta Ufficiale dell’Unione Europea L404: 9-24.
7. EFSA Scientific Committee. Guidance on safety assessment of botanicals and botanical preparations intended for use as ingredients in food supplements. EFSA Journal 2009;7:1249.
8. Sanzini E, Badea M, Dos Santos A, et al. Quality control of plant food supplements. Food & Function 2012;2:740-6.
9. Di Lorenzo C, Dopter A, Vecchio S, et al. The other face of the moon: side effects, interactions and molecules of concerns. In: Food supplements containing botanicals: Benefits, side effects and regulatory aspects. The scientific inheritance of the EU Project PlantLIBRA, P. Restani Editor. Springer International Publishing AG, 2018:141-76.
10. Di Lorenzo C, Ceschi A, Kupferschmidt H, et al. Adverse effects of plant food supplements and botanical preparations: a systematic review with critical evaluation of causality. Br J Clin Pharmacol 2014;79:578-92.
11. Lüde S, Vecchio S, Sinno-Tellier S, et al. Adverse effects of plant food supplements and plant consumed as food: results from the poisons centres-based PlantLIBRA study. Phytother Res 2016;30(6):988-96.
12. EMA 2013. Assessment report on Camellia sinensis (L.) Kuntze, non fermentatum folium. EMA/HMPC/283629/2012, published 12 Novembre 2013. Disponibile a: www.ema.europa.eu/en/documents/herbal-report/final-assessment-report-camellia-sinensis-l-kuntze- non-fermentatum-folium_en.pdf
13. Mak JC. Potential role of green tea catechins in various disease therapies: progress and promise. Clin Exp Pharmacol Physiol 2012;39:265-73.
14. EFSA. Scientific opinion on the substantiation of health claims related to various food(s)/food
constituent(s) claiming biotrasformation of xenobiotic substances (ID 1378, 2388, 2401, 3900, 3942,
4039, 4510, 4513, 4544, 4628, 4639), “elimination”, “cleansing” and “purification” (ID 1347, 4024, 4442, 4457), elimination of heavy metals (ID 1887, 3156), and maintenance of normal bowel function (ID4039) pursuant to Article 13(1) of Regulation (EC) No 1924/2006. EFSA Journal 2010;8(10):1733.
15. EFSA. Scientific opinion on the safety of green tea catechin. EFSA Journal 2018;16(4):5239.
16. Suntar I, Khan H, Patel S, et al. An overview on Citrus aurantium L.: Its functions as food ingredients and therapeutic agent. Oxid Med Cell Longev 2018;2018:7864269.
17. Peters CM, O’neill JO, Young JB, Bott-Silverman C. Is there association between ephedra and hearth failure? A case series. J Cardiac Fail 2005;11:9-11.
18. EMA 2015. European Union herbal monograph on Ginkgo biloba L. folium. Disponibile a: www.ema.europa.eu/en/documents/herbal-monograph/final-european-union-herbal-monograph-ginkgo- biloba-l-folium_en.pdf
19. EMA 2015. Ginkgo foglia. Disponibile a: www.ema.europa.eu/en/documents/herbal-summary/ginkgo- leaf-summary-public_it.pdf.
20. EMA 2009. Community herbal monograph on Hypericum perforatum, herba (Traditional use). www.ema.europa.eu/en/documents/herbal-monograph/final-community-herbal-monograph-hypericum- perforatum-l-herba-well-established-medicinal-use_en.pdf.
21. EMA 2009. Assessment report on Hypericum perforatum L, herba. www.ema.europa.eu/en/documents/herbal-monograph/final-community-herbal-monograph-hypericum- perforatum-l-herba-traditional-use_en.pdf.
22. NIH 2019. Hypericin. Disponibile a: pubchem.ncbi.nlm.nih.gov/compound/hypericin.
23. NIH 2019. Hyperforin. Disponibile a: pubchem.ncbi.nlm.nih.gov/compound/Hyperforin.