L’assorbimento orale dei principi attivi (PI) è influenzato da diversi fattori che determinano la quantità di PI che raggiunge la circolazione sanguigna.
Questi fattori includono il rate di dissoluzione nei liquidi corporei, la permeabilità della membrana gastrointestinale, il rilascio del principio attivo dalla forma farmaceutica, la velocità dello svuotamento gastrico e il metabolismo intestinale.
I principi attivi ingeriti attraversano il tratto gastrointestinale, iniziando dall’esofago con movimenti peristaltici che spingono il farmaco verso lo stomaco, dove il tempo di permanenza varia da 5 minuti a 2 ore, influenzato dalle dimensioni delle particelle.
Nel piccolo intestino, responsabile della maggior parte dell’assorbimento dei nutrienti, il tempo di transito è di circa 3-4 ore, essenziale per la biodisponibilità, soprattutto quelli a rilascio prolungato.
Il colon, la parte finale del tratto gastrointestinale, ha un tempo di transito variabile da 12 a 36 ore, dove assorbe acqua e sostanze, compattando le feci. Questi fattori sono cruciali per l’efficacia dell’assorbimento dei principi attivi e devono essere considerati nella progettazione delle formulazioni farmaceutiche per garantire un’adeguata biodisponibilità.
L’acido alfa-lipoico (ALA), noto per le sue proprietà antiossidanti, è ampiamente utilizzato in ambito clinico ma la sua efficacia è limitata dalla sua biodisponibilità, solo del 30% a causa di un’elevata metabolizzazione prima del raggiungimento della circolazione sistemica.
Nonostante sia rapidamente assorbito, l’assunzione di ALA è influenzata dalla presenza di cibo che ne riduce l’assorbimento. Attraversa la barriera emato-encefalica e agisce come antiossidante diretto e indiretto, neutralizzando specie ossidanti dell’ossigeno e formando complessi chelanti con metalli di transizione.
L’ALA induce anche l’espressione dell’enzima emeossigenasi 1 (HO-1), suggerendo un ulteriore meccanismo di protezione cellulare, potenzialmente anti-infiammatorio. Migliorare la biodisponibilità di ALA è cruciale per garantire concentrazioni plasmatiche ottimali e massimizzare i suoi effetti farmacodinamici.
L’assorbimento di ALA può variare con l’età e non è significativamente influenzato dal tempo di svuotamento gastrico.
Tuttavia, la sua instabilità chimica e la tendenza alla polimerizzazione rappresentano sfide per il miglioramento della sua biodisponibilità. Strategie per migliorare l’assorbimento includono l’utilizzo di tecnologie che stabilizzano il principio attivo, garantendone un rilascio più efficace e controllato.
Tecnologia Physio Release®
La Tecnologia Physio Release® rappresenta un avanzamento significativo nei sistemi di rilascio controllato di principi attivi per somministrazione orale. Rispetto ai metodi tradizionali che comportano la preparazione di compresse con rilascio modificato, questa tecnologia unisce il principio attivo a eccipienti inerti in un conglomerato compresso. Questi eccipienti sono appositamente selezionati per regolare il rilascio del principio attivo in modo specifico:
- Velocità: La velocità di rilascio del principio attivo può essere rallentata per ridurre la frequenza delle somministrazioni.
- Tempo: Il rilascio può essere ritardato in modo che inizi dopo un certo periodo dall’assunzione.
- Sito: Il principio attivo può essere rilasciato in una specifica parte del tratto gastrointestinale, come l’intestino tenue.
L’obiettivo primario della Tecnologia Physio Release® è garantire un assorbimento costante nel tempo, mantenendo livelli ematici del principio attivo all’interno dell’intervallo terapeutico desiderato. Inoltre, essa mira a rendere il principio attivo disponibile per l’assorbimento solo nelle zone in cui può avvenire efficacemente, come l’intestino tenue, prevenendone il rilascio e la possibile degradazione in altre parti del tratto gastrointestinale, come il colon.
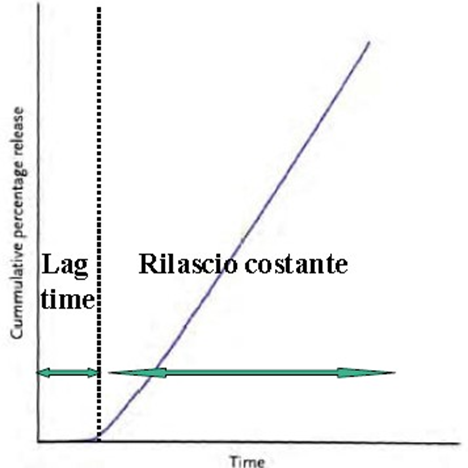
Una volta assunta a stomaco vuoto, la compressa inizia a dissolversi dopo circa 30 minuti dall’ingestione, quando si trova nell’intestino tenue. Questo processo di dissoluzione continua per circa 4 ore, permettendo al principio attivo di essere completamente rilasciato nei liquidi organici dell’intestino tenue e garantendo che non raggiunga il colon dove non sarebbe più assorbito.
Con Physio Release®, il tempo e il sito di rilascio del principio attivo possono essere regolati per massimizzare i benefici terapeutici
Bibliografia:
Custodio, J.M., Wu Chi-Yuan, Benet, L. (2008) Predicting drug disposition, absorption/elimination/ transporter interplay and the role o ood on drug absorption.
Advanced Drug Delivery Reviews, 60, 717–733. Davit, B., Conner, D. (2008) Food e ects on drug bioavailability: Implications or new and generic drug development. In: Krishna, R., Yu, L. (eds)
Biopharmaceutics Applications in Drug Development. Springer, New York.
Fleisher, D., Sweet, B.V., Parekh, A., Boullata, J.I. (2010) Drug Absoprtion with Food. In: Handbook of Drug Nutrient Interactions, Nutrition and Health, Part 3, 209–241. Humana Press, Springer, New York.
Gray, V., Dressman, J. (1996) Change o pH requirements or simulated intestinal f uid TS. Pharmacopeial Forum, 22, 1943–1945.
Dobson, P.D., Kell, D.B. (2008) Carrier-mediated cellular uptake o pharmaceutical drugs: an exception or the rule? Nature Drug Discovery Reviews, 7, 205–220.
Hu, M., Li, X. (eds) (2011) Bioavailability: Basic Principles, Advanced Concepts, and Applications. John Wiley & Sons, New Jersey.
McConnell, E.L., Fadda, H.M., Basit, A.W. (2008) Gut instincts: Explorations in intestinal physiology and drug delivery. International Journal of Pharmaceutics, 34, 213–226.
Sugano, K., Kansy, M., Artursson, P., Avdee , A., Bendels,
S., Di, L., et al. (2010) Coexistence o passive and
carrier-mediated processes in transport. Nature Reviews Drug Discovery, 9, 597–614.
Rochette L, Ghibu S, Richard C, et al. Direct and indirect antioxidant properties of
α-lipoic acid and therapeutic potential. Mol Nutr Food Res 2013;57:114-25.
2 Teichert J, Hermann R, Ruus P, et al. Plasma kinetics, metabolism, and urinary excretion
of alpha-lipoic acid following oral administration in healthy volunteers. J Clin Pharmacol 2003;43:1257-67.
3 Teichert J, Tuemmers T, Achenbach H, et al. Pharmacokinetics of alpha-lipoic acid in subjects with severe kidney damage and end-stage renal disease. J Clin Pharmacol 2005;45:313-28.
4 Mignini F, Nasuti C, Gioventu G, et al. Human bioavailability and pharmacokinetic
profile of different formulations delivering alpha lipoic acid. Journal of Bioequivalence and Bioavailability 2012;1:1-6.
5 Keith DJ, Butler JA, Bemer B, et al. Age and gender dependent bioavailability of R- and R,S-α-lipoic acid: a pilot study. Pharmacol Res 2012;66:199-206.
6 Koufaki M. Therapeutic applications of lipoic acid: a patent review (2011 – 2014). Expert Opin Ther Pat 2014;24:993-1005.
7 Kisanuki A, Kimpara Y, Oikado Y, et al. Ringopening polymerization of lipoic acid and
characterization of the polymer. Journal of Polymer Science Part A: Polymer Chemistry 2010;48:5247-53.
8 Carlson DA, Smith AR, Fischer SJ, et al. The plasma pharmacokinetics of R-(+)-lipoic acid administered as sodium R-(+)-lipoate to healthy human subjects. Altern Med Rev 2007;12:343-51.