Come cambiano le linee guida sulla pubblicità dei dispositivi medici a base di sostanze e quali sono gli impatti per aziende e professionisti del settore
La disciplina sulla pubblicità dei dispositivi medici a base di sostanze ha subito un’importante riorganizzazione con l’approvazione delle nuove linee guida del Ministero della Salute (aprile 2025). Sebbene il regime autorizzativo resti simile a quello precedente, il contesto normativo è stato aggiornato in base ai regolamenti europei MDR e IVDR e ai decreti legislativi nazionali del 2022.
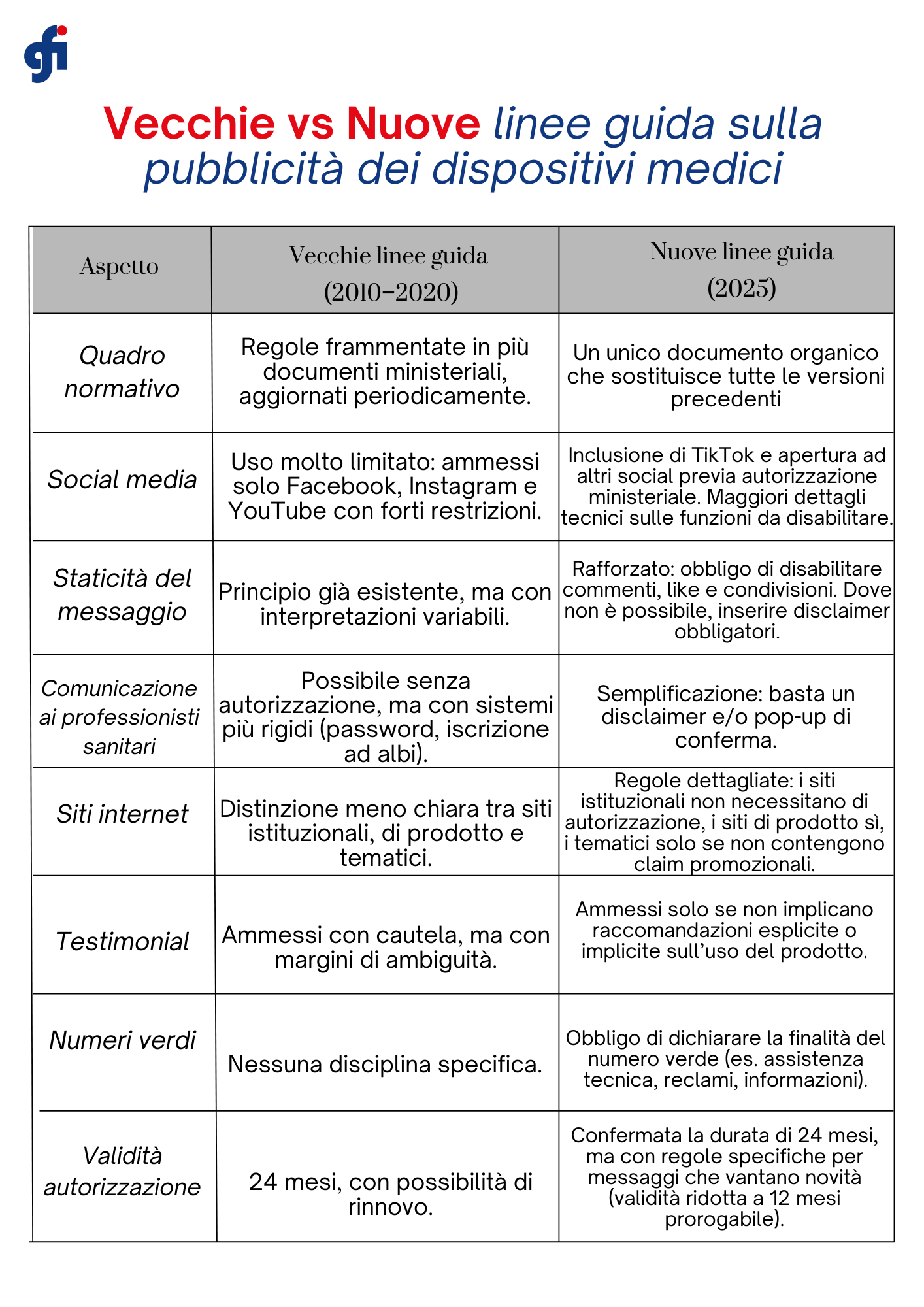
Il documento raccoglie in un unico testo le prescrizioni emanate negli ultimi quindici anni, sostituendo le precedenti linee guida (2010–2020). L’obiettivo è garantire maggiore chiarezza agli operatori del settore e, al contempo, assicurare trasparenza e tutela della salute pubblica.
Social media e staticità del messaggio
Un punto centrale riguarda l’utilizzo dei social network. È confermato il divieto generale di promuovere dispositivi medici tramite canali che permettano modifiche al messaggio autorizzato, come commenti o condivisioni. Tuttavia, le nuove linee guida introducono aperture importanti:
- TikTok entra tra i canali consentiti, purché siano disabilitate funzioni interattive come commenti, “duetti” e “stitch”.
- Rimane valida la possibilità di usare Facebook, Instagram e YouTube con limitazioni tecniche (ad esempio disabilitazione dei like e dei commenti visibili).
- È ammesso l’uso di link attivabili che rimandano a contenuti già autorizzati o a pagine di educazione sanitaria che non necessitano di autorizzazione.
L’introduzione di TikTok segna un’evoluzione rilevante: la comunicazione dei dispositivi medici a base di sostanze si apre a piattaforme frequentate da un pubblico più giovane, mantenendo comunque il principio di staticità del messaggio.
LinkedIn: il grande assente nelle nuove linee guida
Le nuove linee guida ministeriali non menzionano LinkedIn tra i social network autorizzabili. Probabilmente la scelta deriva dal fatto che la piattaforma sia considerata uno strumento dedicato principalmente a professionisti e operatori del settore, quindi meno esposta al rischio di pubblicità ingannevole verso il consumatore finale. Tuttavia, questa esclusione solleva interrogativi: LinkedIn è oggi sempre più utilizzato dalle aziende anche per campagne di comunicazione istituzionale e branded content, creando un’area grigia che richiederà chiarimenti futuri per non penalizzare la comunicazione B2B.
Comunicazione ai professionisti sanitari
Le nuove regole ribadiscono che i messaggi rivolti esclusivamente ai professionisti sanitari non necessitano di autorizzazione. Per distinguere chiaramente questi contenuti da quelli destinati al pubblico, le aziende devono adottare strumenti come:
- Disclaimer specifici, che dichiarino l’esclusiva destinazione agli operatori sanitari;
- Pop-up di accesso, con cui l’utente conferma di appartenere alla categoria professionale.
Questo approccio elimina la necessità di verifiche più rigide, come la richiesta di password o iscrizione ad albi, considerate ormai obsolete.
Siti internet e distinzione dei contenuti
Le linee guida distinguono nettamente tra tre tipologie di siti:
- Siti istituzionali aziendali: non necessitano di autorizzazione se non contengono riferimenti promozionali ai dispositivi.
- Siti di prodotto: richiedono autorizzazione ministeriale per qualsiasi contenuto pubblicitario, incluse immagini e descrizioni.
- Siti tematici: consentiti senza autorizzazione se hanno finalità divulgative e non vantano proprietà specifiche di un dispositivo.
In ogni caso, la responsabilità della richiesta di autorizzazione resta in capo all’azienda promotrice.
Testimonial, numeri verdi e altri dettagli operativi
Un altro aspetto aggiornato riguarda l’uso dei testimonial: è ammesso solo se la loro presenza non implica raccomandazioni dirette o implicite sull’uso del dispositivo. Inoltre, i messaggi che includono numeri verdi devono specificare chiaramente la finalità (es. assistenza tecnica, punti vendita) per evitare usi impropri a fini promozionali.
Conclusioni: opportunità e responsabilità per le aziende
Per i produttori e distributori di dispositivi medici a base di sostanze, le nuove linee guida rappresentano al tempo stesso un vincolo e un’opportunità. Da un lato impongono regole più stringenti sulla staticità dei messaggi e sull’uso dei social network; dall’altro, aprono a nuovi canali digitali e offrono maggiore chiarezza operativa.
Siamo il tuo partner strategico per lo sviluppo e la produzione di soluzioni nutraceutiche e cosmetiche.
Offriamo servizi completi di Contract Development and Manufacturing (CDMO e produzione conto terzi) per l’ideazione, la produzione e la commercializzazione di:
- Integratori alimentari
- Dispositivi medici a base di sostanze
- Dermocosmetici
Le nostre soluzioni includono Private Label, Out-licensing e un servizio Ready-to-Market che garantisce efficienza e rapidità. Ogni progetto è gestito con la massima attenzione alla qualità, all’innovazione e alla conformità regolatoria, supportandoti fino alla fase di distribuzione.
Fonti: Ministero della Salute – Linee guida sulla pubblicità sanitaria dei dispositivi medici, dispositivi medico-diagnostici in vitro e presidi medico-chirurgici (02 aprile 2025). Documento ufficiale che sostituisce tutte le precedenti linee guida del 2010, 2013, 2017, 2019 e 2020