Quando si parla di nutraceutica si parla di una scienza che intende promuovere la salute umana mediante l’uso di nutrienti e di prodotti a formulazione piu o meno complessa. La difficolta nell’orientamento del settore della nutraceutica sta nel fatto che non esiste una categoria commerciale con il nome specifico (in pratica non esiste legalmente il “nutraceutico”), ma ci si deve avvalere di prodotti variamente classificati e regolamentati da diverse legislazioni nazionali ed internazionali [1, 2]. I prodotti associabili alla nutraceutica possono essere normati dalla legislazione alimentare o da quella del farmaco; conseguentemente le caratteristiche di qualita della materia prima e la composizione del prodotto finito possono variare, cosi come puo essere significativamente diversa la documentazione scientifica richiesta per la commercializzazione. Alla legislazione alimentare fanno riferimento gli alimenti funzionali (o arricchiti) e gli integratori alimentari. Nella normativa del farmaco rientrano i farmaci veri e propri, quali i complessi vitaminici ad alto dosaggio o estratti vegetali usati a scopo terapeutico/ funzionale (valeriana), e i farmaci della cosiddetta medicina tradizionale/alternativa che possono essere usati senza prescrizione medica e sono comunemente a base di estratti vegetali.
Qualità e sicurezza nel settore della nutraceutica
Quando parliamo di qualita di un prodotto dobbiamo differenziare chiaramente l’utilizzatore finale dello stesso, ovvero tenere ben presente se la popolazione di riferimento e quella generale o si parla di fasce a rischio, quali i pazienti con varie patologie o i consumatori portatori di specifiche esigenze alimentari (soggetti allergici o con intolleranze). I principali aspetti da monitorare nel controllo di qualita sono:
a. composizione del prodotto (ingredientistica e relativa idoneita all’obiettivo preposto);
b. rispondenza ai requisiti richiesti, ad esempio nel caso di un prodotto in cui si dichiari l’assenza di un allergene tale affermazione deve essere comprovata da opportune metodologie analitiche;
c. presenza di contaminanti di origine biologica, quali la carica batterica patogena e non, le tossine batteriche e le micotossine;
d. presenza di contaminanti ambientali, quali metalli pesanti o inquinanti di origine industriale (diossine, ftalati, ecc.);
e. presenza di contaminanti derivanti dalle pratiche agricole o zootecniche, quali la presenza di residui di prodotti fitosanitari o farmaci veterinari;
f. presenza di contaminanti accidentali anche se di difficile identificazione;
g. contraffazioni e aggiunte illecite.
Composizione del prodotto e relativa rispondenza ai requisiti “funzionali” attesi
I prodotti inclusi nella categoria dei farmaci devono seguire rigorosissime norme di manifattura e quindi difficilmente (anche se ci sono state le dovute eccezioni) si riscontrano problemi di composizione. Molto piu complessa e la situazione dei farmaci di medicina tradizionale o dei prodotti del settore alimentare in cui le norme, pur severe, possono risultare piu frequentemente disattese. Questo fatto puo dipendere:
1) dal numero elevatissimo di prodotti sul mercato, che nel caso degli integratori raggiunge le migliaia;
2) dall’elevato numero di aziende produttrici e distributrici;
3) dalla provenienza internazionale (a volte poco tracciabile) delle materie prime o dei prodotti finiti, ecc.
Ci sono differenze sostanziali nelle caratteristiche di qualita dei prodotti inclusi nel settore della nutraceutica. I prodotti a base di vitamine e minerali sono solitamente meglio controllabili e di conseguenza meno frequentemente implicati in anomalie compositive o nel superamento dei limiti di contaminanti ammessi; viceversa risultano molto piu a rischio quei prodotti in cui l’ingrediente o gli ingredienti attivi sono rappresentati da estratti di origine vegetale (botanicals) o animale (bava di lumaca, cartilagine di squalo, ecc.) [3]. Relativamente alla dimostrazione che il prodotto possa apportare i benefici promessi, ci sono diversi aspetti da considerare; innanzi tutto sarebbe importante corredare il prodotto di un certificato di analisi che dimostri presenza, abbondanza e sicurezza delle molecole attive previste nel prodotto destinato al consumatore [4, 5]. Inoltre, per vantare specifiche indicazioni di salute (claims salutistici) sono necessari studi che dimostrino inequivocabilmente l’attivita biologica utilizzando test in vitro e in vivo, secondo quanto richiesto dagli organismi di riferimento nazionali (Ministero della Salute) ed internazionali (European Food Safety Authority, Food and Drug Administration, Joint Expert Committee on Food Additives, ecc.). Nel caso dei botanicals ci sono due aspetti importanti nel controllo di qualita: la loro autenticazione e standardizzazione. Nel primo caso si deve verificare la corretta identificazione della pianta e della parte da cui si otterra l’estratto; parti diverse di una pianta possono avere composizione e talora tossicita totalmente diversa. Gli approcci analitici utilizzabili per la caratterizzazione e standardizzazione della materia prima sono molto diversi: da metodi di screening rapidi, quali ad esempio la cromatografia su strato sottile o l’analisi del DNA (DNA fingerprint) a metodiche estremamente sensibili e complesse per la caratterizzazione/standardizzazione delle molecole attive (cromatografia liquida accoppiata a vari detectors, incluso lo spettrometro di massa).

Nella Figura 1 viene illustrato un esempio di screening rapido per il riconoscimento di estratti da specie diverse di Citrus mediante cromatografia su strato sottile ad alta prestazione (high performance thin layer chromatography, HPTLC); tutti gli estratti inclusi nella separazione sono ammessi quali ingredienti di integratori alimentari, ma in base alla diversa composizione e attivita fisiologica non e possibile un loro uso alternativo. In particolare, il Citrus aurantium contiene ammine attive con potenziale tossico (pertanto regolamentate), non presenti in quantita apprezzabili nelle altre specie. Come e possibile evidenziare in Figura 1, la corsa cromatografica del campione di limone (con entrambe le rilevazioni) e decisamente diverso da quelli dei due campioni di arancio, apparentemente simili. E pero possibile distinguere l’arancio dolce (Citrus sinensis) dall’arancio amaro (Citrus aurantium) grazie alle due bande indicate da frecce nell’immagine di sinistra ottenuta per esposizione della lastrina a 366 nm. Il secondo aspetto da tener presente e la standardizzazione degli estratti, il cui scopo e quello di poter offrire al consumatore un prodotto stabile nel tempo sia in termini di controllo dei contaminanti sia per il contenuto di molecole ritenute responsabili delle proprieta biologiche e fisiologiche [6].
Presenza di sostanze pericolose per la popolazione generale o per gruppi di consumatori “a rischio”
Sembra strano ma l’attuale sistema di qualita della filiera alimentare nasce da preoccupazioni sollevate dalla NASA negli anni ’60. Infatti, questo ente si poneva il problema di assicurare l’assenza di contaminanti pericolosi (microrganismi ed altre sostanze tossiche) negli alimenti destinati alle missioni spaziali. Da allora molta strada e stata fatta e l’applicazione delle norme HACCP (Hazard-Analysis and Critical Control Points) e ormai richiesta a qualunque azienda lavori nel settore alimentare. L’HACCP consiste nell’istituzione di un insieme di procedure di produzione di un alimento (dalla materia prima al prodotto finito), volte a prevenire i potenziali rischi per il consumatore. Come detto prima, i prodotti utilizzati in nutraceutica sono per lo piu classificati quali integratori e vengono pertanto normati dagli stessi regolamenti del settore alimentare. In questo contesto devono pertanto anche assicurare il controllo degli ingredienti allergenici (soia, arachide, sesamo, ecc.) o implicati nelle intolleranze alimentari (lattosio, ecc.).
Dal momento che i prodotti usati nella nutraceutica spesso contengono ingredienti di origine vegetale, e importante tenere sotto controllo alcune categorie di contaminanti potenzialmente a rischio per la salute umana. Innanzi tutto devono essere tenuti sotto controllo la carica batterica, le muffe e il contenuto di tossine che ne derivano. Tra i contaminanti microbiologici piu frequentemente riportati nelle allerte europee, possiamo citare in ordine decrescente di importanza: la Salmonella typhimurium, l’Escherichia coli, la Listeria monocytogenes e il Bacillus cereus [8]. Anche le micotossine devono essere monitorate, in quanto presentano un potenziale tossico elevato; ad esempio, l’associazione tra assunzione di aflatossine e tumori del fegato nell’uomo e documentato da diversi studi epidemiologici condotti soprattutto nei Paesi in via di sviluppo, dove la concentrazione di queste tossine negli alimenti puo raggiungere valori elevati [7]. Il controllo delle micotossine viene comunemente effettuato dalle aziende produttrici; non si puo pero tacere la difficolta del controllo stesso a causa della matrice (gli ingredienti complessi della formulazione) che puo “mascherare” o legare le micotossine rendendole meno estraibili. Inoltre, dal momento che derivano dalla presenza di muffe, e frequente la contaminazione “a macchia di leopardo”, che comporta la necessita di definire attentamente i piani di campionamento [9].
Le micotossine piu frequentemente segnalate nelle allerte europee sono le aflatossine, lo zearalenone e il deossinivalenolo (DON) [8]. Per quel che riguarda i metalli pesanti, la contaminazione puo avere due principali origini: la presenza naturale nel suolo o la loro dispersione nell’ambiente da parte delle attivita antropiche. Certamente il caso meglio conosciuto e quello del mercurio, che puo pervenire agli alimenti sia per contaminazione dell’ambiente a seguito di rilascio da siti industriali, sia per la sua presenza naturale, come nel caso del Bacino del Mediterraneo sul cui fondo passa una fascia di cinabro (solfuro di mercurio) [10]. Altri metalli particolarmente tossici per l’uomo sono il piombo, il cadmio, l’arsenico, ecc. Anche se i derivati vegetali sono relativamente meno soggetti di quelli animali alla presenza di alte concentrazioni di metalli pesanti (nell’animale esiste il fenomeno della bioconcentrazione), non va dimenticato che alcuni prodotti della medicina ayurvedica ne possono contenere quantita significative e sufficienti ad indurre eventi tossici nel consumatore [11].
Due ulteriori gruppi di contaminanti da tenere sotto controllo sono i residui di prodotti fitosanitari (comunemente chiamati pesticidi) e di farmaci veterinari, entrambi normati da legislazioni nazionali e internazionali. Parlando di prodotti per la nutraceutica, e quindi per lo piu contenenti estratti vegetali, si tratteranno di seguito in maggior dettaglio le problematiche derivanti dai prodotti fitosanitari. I prodotti fitosanitari sono classi di molecole utilizzate per proteggere le colture da malattie o organismi dannosi; i principali sono gli insetticidi, i fungicidi e i diserbanti. Questi prodotti devono seguire rigorose norme di utilizzo che vengono definite nel loro complesso Buone Pratiche Agricole (Good Agricultural Practices, GAP). Le GAP prevedono dosaggi e tempi di sospensione (tempo tra trattamento e raccolta) in grado di ridurre al minimo la presenza di residui. Sebbene una agricoltura convenzionale ben condotta non presenti rischi per i consumatori, spesso si preferisce coltivare secondo agricoltura biologica le piante destinate alla produzione di estratti. Qualunque sia l’approccio agronomico scelto, le materie prime devono essere accuratamente analizzate per verificarne la qualita sia in termini di residui di prodotti fitosanitari nei prodotti convenzionali sia di un eventuale incremento di contaminazione da micotossine qualora si scelga l’approccio biologico [12].
Ottimizzazione della formulazione dei prodotti utilizzati nel settore della nutraceutica
La verifica della materia prima rappresenta solo il primo punto critico nel controllo di qualita di un prodotto destinato al mercato della nutraceutica. Innanzi tutto, solo una parte dei prodotti e monoingrediente; la maggioranza degli integratori alimentari, infatti, contiene piu ingredienti attivi che nel caso degli estratti vegetali possono inficiare l’efficienza delle metodiche analitiche utilizzate dall’azienda produttrice e dagli enti di controllo che sono responsabili del monitoraggio del mercato. In questo senso sono richieste competenze specifiche e alcune metodiche ufficiali, validate su miscele di molecole purificate, possono risultare inidonee all’analisi delle stesse in matrici complesse. Una problematica di questo genere e sorta quando la normativa ha esteso i limiti negli integratori alimentari a tutte le ammine attive del Citrus aurantium (in precedenza era regolamentata solo la sinefrina); si e infatti osservato che la metodica comunemente utilizzata non era in grado di quantificare le cinque ammine attive nei prodotti finiti, in quanto il tracciato cromatografico non risultava sufficientemente risolto [13]. La separazione (e quantificazione) delle cinque principali ammine del Citrus aurantium (sinefrina, octopamina, tiramina, N-metil-tiramina e ordenina) e stata possibile con la modifica di una metodica analitica precedentemente pubblicata [14]. La Figura 2 evidenzia quanto riportato sopra, ovvero:
- La migliore risoluzione degli analiti ottenuta con il nuovo metodo; in maggior dettaglio, confrontando i cromatogrammi della miscela delle 5 ammine del Citrus aurantium ottenuti con il metodo di Putzbach et al. [13] (pannello A) e con il metodo modificato (pannello B), si puo apprezzare il miglioramento della separazione pur
con una riduzione significativa dei tempi di analisi.
- La migliore separazione ottenuta con il nuovo metodo, che permette una migliore quantificazione nel campione sia con il detector UV (pannello D verso C) sia con quello fluorimetrico (pannello F verso E), pur con l’iniezione di un volume di campione dimezzato nel secondo caso (5 contro 10 μL).
- L’effetto matrice di cui si e precedentemente parlato, evidente nel pannello C; questo problema risulta molto meno problematico con il metodo di Di Lorenzo et al. [14] (pannelli D e F).

Dal momento che la sinefrina e le altre ammine attive del C. aurantium sono regolamentate negli integratori alimentari con un limite che non deve essere superato con la dose giornaliera, e evidente l’importanza di avere a disposizione una metodica analitica affidabile. Solo un metodo validato sul prodotto finito puo permettere un corretto controllo di qualita per l’azienda produttrice e un monitoraggio efficace del mercato. Il caso del C. aurantium e stato qui trattato come esempio delle difficolta analitiche nel settore, che si incontrano tanto piu frequentemente quanto piu e complessa la formulazione del prodotto.
Contaminazioni accidentali, contraffazione e aggiunte illecite
Il settore del farmaco convenzionale, pur non esente, e meno frequentemente oggetto di azioni fraudolente anche per le immediate conseguenze che si manifesterebbero in un paziente in terapia. Molto piu appetibile e il mercato dei prodotti utilizzati nella medicina tradizionale e degli integratori alimentari. In questi casi la commercializzazione richiede una minore documentazione scientifica e l’utilizzo e per lo piu deciso dal consumatore (integratore alimentare) o da “professionisti” che non appartengono alla medicina convenzionale. Nel caso degli integratori alimentari si parla di effetti fisiologici o salutistici che raramente sono monitorati con misure di biomarker o verifica della salute del consumatore. Non va poi dimenticato l’aspetto psicosomatico, derivante dalla convinzione diffusa che tutto ciò che è naturale può solo fare bene; quindi e difficile che eventi avversi vengano associati dal consumatore a prodotti contenenti botanicals. E invece noto che problemi importanti per la sicurezza del consumatore possono derivare sia da contaminazioni accidentali sia da vere e proprie azioni criminali.
Contaminazioni accidentali
Tra le contaminazioni accidentali piu preoccupanti, vanno sicuramente citate le piante che producono alcaloidi pirrolizidinici. Piu di 600 alcaloidi appartenenti a questa classe sono stati identificati in piu di 6.000 piante; almeno la meta di queste molecole e potenzialmente epatotossica e cancerogenica. La grande diffusione delle piante contenenti queste molecole in tutti i continenti determina un rischio concreto di contaminazione accidentale di altre piante utilizzate per la mangimistica e l’alimentazione umana [15]. Uno studio condotto in Germania ha dimostrato che il livello di alcaloidi pirrolizidinici dosati in 169 tisane contenenti ingredienti vegetali (camomilla, ortica, finocchio, melissa e menta) oscillava tra 0 e 5668 μg/kg di prodotto secco [16]. In tre casi, utilizzando i valori analitici ottenuti, il consumo di infuso nelle quantita giornaliere medie portava al superamento dei livelli raccomandati dal German Federal Institute for Risk Assessement (BfR), ovvero di 0,007 μg/kg di peso corporeo equivalente a 0,42 μg per un peso di 60 kg. Un altro caso, che ha creato numerosi problemi sul mercato Italiano, consisteva nella contaminazione di un lotto di Coleus forskohlii (Willd.) incluso come ingrediente in diverse tipologie di prodotti: integratori alimentari, preparazioni galeniche, prodotti per lo sportivo, ecc. Da tempo usato nella medicina ayurvedica, il Coleus forskohlii e recentemente entrato a far parte degli ingredienti che promuoverebbero la lipolisi e la termogenesi, con conseguente supposto potere dimagrante. Nella primavera del 2005, alcuni soggetti erano pervenuti al Pronto Soccorso di diverse citta in stato confusionale, in preda ad allucinazioni, secchezza delle fauci, midriasi, amnesia retrograda ed altri sintomi tipici dei farmaci anticolinergici [17]. In due soggetti ricoverati, l’evento era stato associato immediatamente al consumo di un integratore alimentare contenente diversi estratti vegetali. Dall’informazione fornita della ditta produttrice, solo per il Coleus forskolhii c’era stata la sostituzione recente del lotto e quindi l’attenzione e stata diretta a questo ingrediente, risalendo all’importatore. L’azienda importatrice aveva regolarmente effettuato l’analisi del lotto mediante HPLC e verificato la presenza e abbondanza della molecola caratterizzante, ovvero la forskolina; il lotto era stato ritenuto nella norma. Considerato che i soggetti intossicati mostravano sintomi anticolinergici, si e ipotizzata la presenza di alcaloidi tropanici (contenuti nelle piante della Famiglia delle Solanaceae, quali Atropa, Datura, ecc.). In breve, utilizzando una metodica idonea all’identificazione degli alcaloidi tropanici, si e evidenziata la presenza di una quantita considerevole di scopolamina e tracce di atropina. L’analisi comunemente impiegata per il controllo del Coleus non era in grado di evidenziare la loro presenza, in quanto eluite con il fronte del solvente. Ai tempi si erano formulate tre ipotesi:
1. Un errore nell’identificazione della materia prima che avrebbe portato, prima dell’estrazione, alla miscela di radici di Coleus con parti botaniche (diverse) provenienti da piante della famiglia delle Solanaceae – questa ipotesi sembrava abbastanza improbabile;
2. Un errore nella preparazione del prodotto finito con miscela di due estratti diversi, uno da Coleus e uno da pianta della famiglia delle Solanaceae (un errore grave considerati il diverso uso e pericolosita delle piante);
3. Sebbene impossibile da dimostrare, si era anche ipotizzata l’aggiunta intenzionale di scopolamina, soprattutto sulla base del fatto che il rapporto tra scopolamina e atropina nel prodotto in esame (9:1) era molto diverso da quello che si trova normalmente in natura (2:1).
L’ipotesi dell’aggiunta intenzionale derivava dalla consapevolezza che in alcuni paesi del Sud America, la scopolamina viene utilizzata in rapine e stupri, per l’amnesia retrograda che induce nelle vittime [18]. Qualora l’ipotesi corretta fosse la terza, il prodotto creato ad hoc per il mercato criminale sarebbe stato inviato all’indirizzo sbagliato!
Contraffazioni e aggiunte illecite
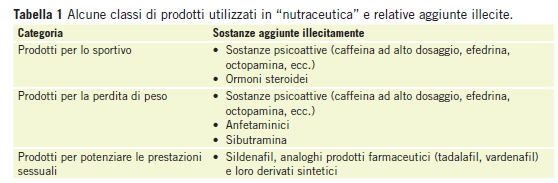
Come detto in precedenza, questo settore e spesso bersaglio di azioni illecite; la contraffazione piu frequente riguarda la sostituzione di un preparato botanico con un’alternativa all’apparenza simile ma di qualita totalmente diversa. I controlli analitici prima descritti diventano quindi fondamentali per tutelare il consumatore dal punto di vista economico (nel migliore dei casi) o di quella della sicurezza se la sostituzione comporta la presenza di sostanze responsabili di possibili eventi avversi [21]. Tra i molti che trattano questo argomento, possono essere citati due lavori recentemente pubblicati, che riportano l’adulterazione di prodotti a base di iperico (Hypericum perforatum L.) con coloranti di sintesi [19] e la sostituzione di fiori di camomilla con quelli di altre specie appartenenti alle Asteraceae [20]. Data la loro diffusione d’uso e l’interesse economico che ne deriva, alcuni estratti botanici risultano particolarmente “appetibili” al mercato della contraffazione e questo e particolarmente vero per alcune categorie di prodotti, in quanto destinate a consumatori che vorrebbero ottenere risultati significativi e rapidi. Come illustrato in Tabella 1, particolare attenzione deve essere rivolta ai prodotti per sportivi, per il controllo del peso corporeo e per l’aumento delle prestazioni sessuali.
Prodotti per lo sportivo: il caso dell’efedrina
Nel mondo della competizione sportiva, il desiderio di migliorare il rendimento psicofisico ha portato in diversi frangenti all’utilizzo di sostanze o pratiche (doping) che possono determinare un grave rischio per la salute degli atleti. L’efedrina e una molecola ad attivita simpaticomimetica che modula in modo diretto ed indiretto il sistema nervoso simpatico. L’efedrina e contenuta in quantita variabile nelle piante del genere Ephedra, il cui uso in passato era alquanto comune negli integratori destinati al controllo del peso (effetto anoressizzante) o nei prodotti per lo sportivo (effetto ergogenico). A seguito di alcuni eventi avversi gravi, tra cui crisi ipertensive e infarto, l’FDA ha vietato nel 2004 l’uso negli integratori alimentari di piante del genere Ephedra e di molecole ad esse associate (efedrina e pseudoefedrina) [22]. Il divieto si e poi esteso in molti altri Paesi, tra cui l’Italia, in quanto si e valutato che i rischi connessi all’utilizzo non terapeutico dell’efedrina superassero di gran lunga i benefici immediati. A seguito di segnalazione di eventi avversi, negli ultimi anni sono stati sottoposti ad analisi numerosi integratori alimentari per i quali si sospettava la presenza di ammine attive non ammesse (efedrina e pseudoefedrina) o, nel caso lo fossero, in quantita piu elevate del consentito (sinefrina e altre ammine del Citrus aurantium). La Figura 3 illustra le fasi analitiche che vengono seguite per il controllo di questi integratori. Innanzi tutto, data la numerosita dei campioni che normalmente vanno sottoposti ad accertamenti (sequestri in depositi o punti vendita) e necessario poter disporre di un metodo di screening. In questo contesto la tecnica dell’HPTLC permette di ottenere in breve tempo un quadro compositivo dei campioni allo studio con identificazione rapida delle “anomalie”.

Per identificare la presenza di ammine attive, sulla lastrina da HPTLC (Figura 3, parte 1), accanto al campione, si caricano gli standard purificati di efedrina, pseudoefedrina, nor-efedrina, sinefrina ed octopamina. I campioni che risultano positivi allo screening vengono quindi sottoposti ad ulteriori accertamenti, mediante HPLC (Figura 3, parte 2) e spettrometria di massa (Figura 3, parte 3). Nei cromatogrammi ottenuti per HPLC e possibile osservare nel campione (parte 2b) un picco con tempo di eluizione identico a quello della efedrina standard (parte 2a). La presenza illecita di efedrina in questo prodotto, la cui analisi e stata utilizzata come esempio, e stata quindi confermata sia con HPLC sia in spettrometria di massa.
Altre anomalie frequenti sono la presenza di prodotti con dosaggio elevato di sinefrina e octopamina, ammine naturalmente presenti nel Citrus aurantium e ammesse ma con limiti ben stabiliti con il dosaggio giornaliero. In diverse situazioni in prodotti per lo sport provenienti da altri Paesi sono state riscontrate elevate concentrazioni di octopamina derivanti da aggiunte della molecola di origine sintetica. Il problema nasce dal fatto che le legislazioni possono variare e non tutti i Paesi considerano l’octopamina una molecola dopante. Ne deriva la messa in commercio di prodotti di importazione non regolari, che vengono fatti divenire tali con la traduzione in Italiano dell’etichetta, in cui si omettono gli ingredienti non ammessi [dati personali non pubblicati].
Prodotti per il controllo del peso corporeo: il caso della sibutramina
Un altro settore in cui il consumatore ricerca un effetto immediato con il minor sforzo possibile e quello dei prodotti destinati alla riduzione del peso corporeo. Come si puo immaginare, l’uso di preparati di origine vegetale non puo certo garantire il raggiungimento rapido di questo obiettivo, a meno che siano presenti molecole attive (efedrina, sinefrina, ecc.) in quantita elevata, che metterebbero comunque a rischio la salute del consumatore. Frequente, specialmente in prodotti provenienti da Paesi extraeuropei, e l’aggiunta di farmaci veri e propri che, non essendo dichiarati, rappresentano un vero problema per le autorita deputate alla tutela della salute del consumatore. Un caso rappresentativo riguarda l’arrivo sul mercato Italiano alcuni anni fa di capsule dimagranti definite “prodotto 100% naturale”, a base di supposti estratti vegetali. La segnalazione di allerta e iniziata su alcuni dati allarmanti segnalati alle autorita sanitarie:
1) il consumatore otteneva un dimagramento consistente e in breve tempo raggiungeva obiettivi non certo attribuibili al contenuto naturale di principi vegetali;
2) le persone che utilizzavano il prodotto presentavano una forma di dipendenza, tipica dei composti chimicamente correlati all’amfetamina;
3) in alcuni casi, si erano osservati effetti avversi di diversa gravita.

La Figura 4 mette in relazione lo spettro di massa ottenuto per infusione diretta in elettrospray del campione in esame e dello standard di sibutramina, entrambi caratterizzati dalla presenza dello ione con 280 m/z. L’ulteriore frammentazione dello ione presente nel campione ha portato a due ioni preponderanti, con m/z 139.05 e 152.90, corrispondenti a quelli riscontrati per frammentazione dello standard. I risultati corrispondevano inequivocabilmente a quelli riportati in letteratura, in quanto l’adulterazione di integratori alimentari con sibutramina erano gia stati segnalati in precedenza [23-25]. Considerando che la sibutramina e stata bandita dall’uso terapeutico per i gravi effetti collaterali che si possono associare ad un consumo protratto nel tempo, va sottolineata l’importanza del monitoraggio di qualita dei prodotti, specialmente quando legati al mercato parallelo (internet, vendita porta a porta, ecc.).
Prodotti per il potenziamento delle prestazioni sessuali: il caso del sidenafil e molecole analoghe
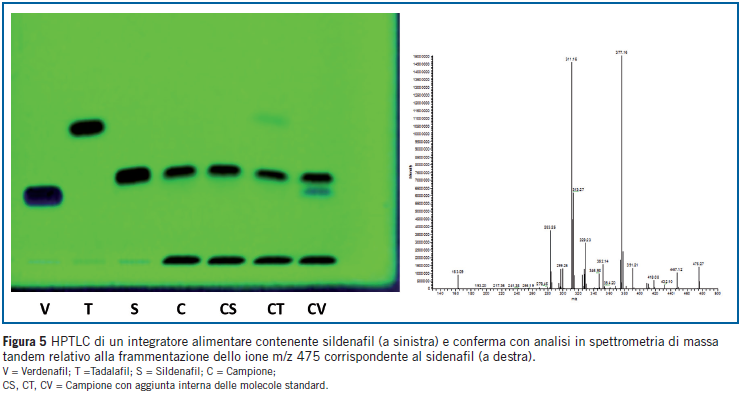
Un’altra classe di prodotti frequentemente oggetto di aggiunte illecite e quella degli integratori che promettono risultati straordinari nelle prestazioni sessuali. Sebbene molte piante siano segnalate per le loro proprieta afrodisiache (Lepidium meyenii o maca; Tribulus terrestris o tribulus, Turnera diffusa o damiana, ecc.) e certo che i prodotti a base esclusivamente di estratti vegetali raramente danno i risultati attesi dalla persona che li utilizza. Molto piu frequentemente gli integratori “tutti naturali” che presentano un’efficacia incontrovertibile contengono sostanze di sintesi. Vengono di seguito descritti due casi di integratori a cui venivano attribuite proprieta energetiche ma che in realta venivano utilizzati come prodotti per disfunzioni erettili. Il primo caso riguarda un integratore di origine extraeuropea definito “tutto vegetale” che vantava proprieta energetiche e afrodisiache. Si e effettuato un primo screening analitico mediante HPTLC, in cui il campione veniva caricato in parallelo alle molecole standard di sildenafil, tadalafil e verdenafil. La Figura 5 mostra la corsa cromatografica del campione, in cui si osserva una banda con Rf (ratio frontis) analogo a quello del sildenafil. L’identificazione della molecola e stata quindi confermata mediante spettrometria di massa e nella Figura 5 viene illustrata in proposito la frammentazione. Il secondo prodotto era rappresentato da un integratore alimentare normalmente commercializzato in Italia, ma segnalato agli organi competenti per una possibile presenza di aggiunte illecite. Anche in questo caso, con il medesimo procedimento analitico, si e pervenuti al riconoscimento di una molecola simile al sildenafil (idrossi-omosildenafil), gia descritta nella letteratura scientifica [3, 26]. E evidente che l’utilizzo di questi “integratori” senza alcun consiglio e controllo medico rappresenta un rischio importante per il consumatore che puo incorrere in eventi avversi severi, ben noti nella letteratura scientifica [27].
Bibliografia
[1] Larranaga-Guetaria A. PlantLIBRA: Plant food supplements, levels of intake, benefit and risk assessment. The regulatory framework for plant
food supplements in the EU. AgroFOOD Industry Hi-Tech. 2012; 23: 20-2.
[2] Silano V, Coppens P, Larranaga-Guetaria A, et al. Regulations applicable to plant food supplements and related products in the European
Union. Food Funct. 2011; 2: 710-9.
[3] Sanzini E, Badea M, Dos Santos A, et al. Quality control of plant food supplements. Food Funct. 2011; 2: 740-6,
[4] SCF (Scientific Committee on Food). Guidance on submissions for safety evaluation of nutrients or of other ingredients proposed for use in the
manufacture of foods. Opinion expressed on 11 July 2001. Scaricabile da: http://ec.europa.eu/food/fs/sc/scf/out100_en.pdf.
[5] EFSA, Food Ingredients and Packaging Unit. Concept paper on the revision of the ‘Guidance on the submissions for safety evaluation of sources
of nutrients or other ingredients proposed for use in the manufacture of foods’. Scaricabile da: https://www.efsa.europa.eu/sites/default/files/
consultation/160608.pdf.
[6] van BreemenRB, Fong HHS, Farnsworth NR. The role of quality assurance and standardization in the safety of botanical dietary supplements.
Chem Res Toxicol. 2007; 20: 577-82.
[7] Hamid AS, Tesfamariam IG, Zhang Y, Zhang ZG. Aflatoxin B1-induced hepatocellular carcinoma in developing countries: Geographical distribution,
mechanism of action and prevention. Oncology Letters. 2013; 5: 1087-92.
[8] Ministero della Salute. Relazione sul sistema di allerta Europeo – anno 2015. Scaricabile da: http://www.salute.gov.it/portale/news/p3_2_1_1_1.
jsp?lingua=italiano&menu=notizie&p=dalministero&id=2447
[9] Gilbert J. Quality assurance in mycotoxin analysis. WHO Publisher, 1999: 33-37. Scaricabile da: http://www.fao.org/3/a-x2100t/X2100t08.pdf
[10] Spada L, Annichiarico C, Cardellicchio N, Giandomenico S, Di Leo A. Mercury and methylmercury concentrations in Mediterranean seafood and
surface sediments, intake evaluation and risk for consumers. International Journal Hygiene and Environmental Health. 2012; 215: 418-26.
[11] Saper RB, Kales SN, Paquin JP et al. Heavy metal content of Ayurvedic herbal medicine products. JAMA. 2004; 292: 2868-73.
[12] Kuzdralinski A, Solarska E, Mazurkiewicz J. Mycotoxin content of organic and conventional oats from southestern Poland. Food Control. 2013;
33: 68-72.
[13] Putzbach K, Rimmer CA, Sharpless KE, Sander LC. Determination of bitter orange alkaloids in dietary supplements standard reference materials
by liquid chromatography with ultraviolet absorbance and fluorescence detection. J. Chromatography A. 2007; 1156: 304-11.
[14] Di Lorenzo C, Dos Santos A, Colombo F et al. Development and validation of HPLC method to measure active amines in plant food supplements
containing Citrus aurantium L. Food Control. 2014; 46: 136-142.
[15] Li N, Xia Q, Ruan J, Fu PP, Lin G. Hepatotoxicity and tumorigenic induced by metabolic activation of pyrrolizidine alkaloids in herbs. Current
Drugs Metabolism 2011; 12: 823-34.
[16] Schulz M, Meins J, Diemert S et al. Detection of pyrrolizidine alkaloids in German licensed herbal medicinal teas. Phytomedicine. 2015; 22:
648-56.
[17] Restani P, Marangon K, Colombo ML. Problemi di controllo qualità e sidurezza di integratori alimentari e preparazioni magistrali contenenti
estratti di Coleus forskholii. In: Cometa MF, Di Consiglio E, Gemma S, Parisi L, Volpe MT editors. “Atti del XIV Congresso Nazionale
della Società Italiana di Tossicologia”. Istituto Superiore di Sanità. 2006; XXIV: 59. Scaricabile da: http://www.iss.it/binary/publ/publi/06_
C1.1138007382.pdf.
[18] Sáiz J, Mai TD, López ML et al. Rapid determination of scopolamine in evidence of recreational and predatory use. Sci Justice. 2013; 53:
409-14.
[19] Frommenwiler DA, Reich E, Sudberg S et al. St. John’s wort versus counterfeit St. John’s Wort: an HPTLC study. J AOAC International. 2016;
99: 1204-12.
[20] Guzelmeric E, Ristivojevic P, Vovk I et al. Quality assessment of marketed chamomille tea products by a validated HPTLC method combined
with multivariate analysis. J Pharm Biomed Anal. 2017: 132: 35-45.
[21] Al Lawati HA, Al Busaidi I, Kadavilpparampu AM, Suliman FO. Determination of common adulterants in herbal medicine and food samples
using Core-shell column coupled to tandem mass spectrometry. J. Chromatogr. Sci. 2017; 55: 232-42.
[22] FDA News Release. 6 February 2004. Scaricabile da: http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/2004/ucm108242.htm
[23] Bae J, Choi C, Jang C, Lee S. Simultaneous determination of sibutramine and its active metabolites in human plasma by LC-MS/MS and its
application to a pharmacokinetic study. Biomed Chromatogr. 2011; 25: 1181-8.
[24] Shi Y, Sun C, Gao B, Sun A. Development of a liquid chromatography tandem mass spectrometry method for simultaneous determination of
eight adulterants in slimming functional foods. J. Chromatography A. 2011; 1218: 7655-62.
[25] Vaysse J, Balayssac S, Gilard V, Desoubdzanne D, Malet- Martino M, Martino R. Analysis of adulterated herbal medicines and dietary supplements
marketed for weight loss by DOSY 1H-NMR. Food Addit Contam Part A Chem Anal Control Expo Risk Assess. 2010; 27: 903-16.
[26] Zou P, Oh SS, Hou P, Low MY, Koh HL. Simultaneous determination of synthetic phosphodiesterase-5 inhibitors found in a dietary supplement
and pre-mixed bulk powders for dietary supplements using high-performance liquid chromatography with diode array detection and liquid
chromatography-electrospray ionization tandem mass spectrometry. J. Chromatography A. 2006; 1104: 113-22.
[27] Cheitlin MD, Hutter AM Jr, Brindis RG et al. ACC/AHA expert consensus document. Use of sildenafil (Viagra) in patients with cardiovascular
disease. American College of Cardiology/American Heart Association. J Am Coll Cardiol. 1999; 33: 273-82.






